
2024年欧洲血液学协会(EHA)年会于当地时间6月13日至16日在西班牙马德里召开,作为全球首屈一指的血液学领域的科学交流盛会,每年都吸引着来自世界各地的专家学者,共同推着血液学科的发展与进步[1]。
弥漫性大B细胞淋巴瘤(DLBCL)是一种来源于成熟B细胞的侵袭性肿瘤,是最常见的
小编节选了一篇“壁报”(P2088),让我们一睹Axicabtagene ciloleucel (Axi-cel)治疗在DLBCL和FL患者中的真实世界安全性。
摘要编号:P2088[6]
英文标题:Real‑World Safety Outcomes of Axicabtagene Ciloleucel in Patients With Diffuse Large B‑Cell Lymphoma and Follicular Lymphoma in Europe and United States: A Systematic Review and Meta‑Analysis
中文标题:在欧洲和美国真实世界中,Axi-cel治疗DLBCL和FL的安全性结局:一项系统综述和荟萃分析
研究背景
自Axi-cel获批用于治疗复发/难治性大B细胞淋巴瘤(R/R LBCL)以来,其安全性真实世界证据(RWE)逐渐增加,其中,欧洲大型国家注册中心报告的安全性RWE的数量显著增加。近年来,全球几项RWE研究记录了不断发展的不良事件管理策略,文献数量的增长为扩展既往对Axi-cel获批适应症的安全性的系统文献综述(SLR)提供了契机。本研究通过分析美国和欧洲的随时间推移的荟萃分析量化证据,报告了Axi-cel治疗在真实世界DLBCL与FL患者中的最新安全性SLR。
研究方法
系统文献检索:在Embase和MEDLINE中检索了2017年及之后发表的符合纳入标准的研究,并手动检索了10个会议的相关摘要。符合纳入标准的研究包括Axi‑cel治疗在R/R DLBCL和/或R/R FL患者中的安全性观察性分析,排除临床试验参与者的病例报告研究。所有文献均由2名独立的审阅者进行严格评估,并遵循系统综述和荟萃分析优先报告的条目,队列mapping将来自同一来源(例如,单个中心或注册中心)的文献合并到同一患者队列中,以2次独立的方式进行数据提取,使用纽卡斯尔-渥太华量表(NOS)评估研究质量。
荟萃分析:证据按地区(美国、欧洲和其他)和时间(以2019年12月为时间临界点,分为2019年12月之前 vs. 2019年12月及之后)整合而成。使用DerSimonian-Laird方法实施随机效应。仅针对不重叠的队列进行荟萃分析,避免重复计算患者,如果同一中心参与多个队列,则仅包括样本量较大的队列。
研究结果
共检索到6972篇文献(包括手动检索的41篇),最终证据库中纳入了73个队列的206篇文献。再排除一个报告亚组预后的队列,最终纳入分析的为72个队列,大多数队列都是回顾性研究队列,几乎所有文献都报告了DLBCL队列,还有一些较新的文献同时包括DLBCL和FL;只有1个队列只包含FL患者。
几篇最新的全文文献来自欧洲注册机构,美国队列通常比欧洲队列开始的更早。总体而言,各队列在筛选和结果上均获得了高质量分数(NOS上的分数均为3),54个队列可获取全文文献或大会幻灯,只有18个队列的报告仅限于摘要。
最终分析中纳入的72个患者队列主要来自美国;其余队列主要来自于欧洲,各有一个队列分别来自中国和加拿大(图1)。一项研究包括来自以色列和美国的患者。
多个单中心队列与多中心注册队列重叠,与美国 CIBMTR 注册队列重叠程度最高。
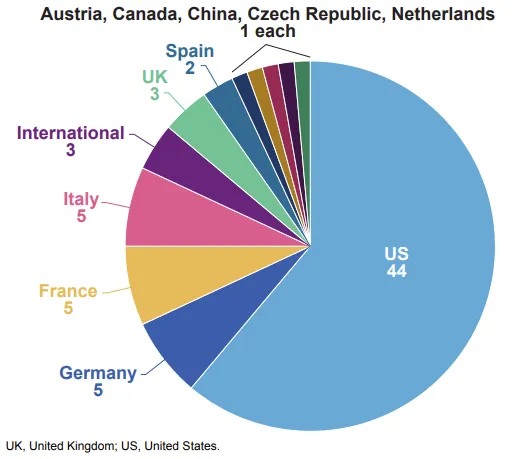
图1 队列在不同国家/地区的分布
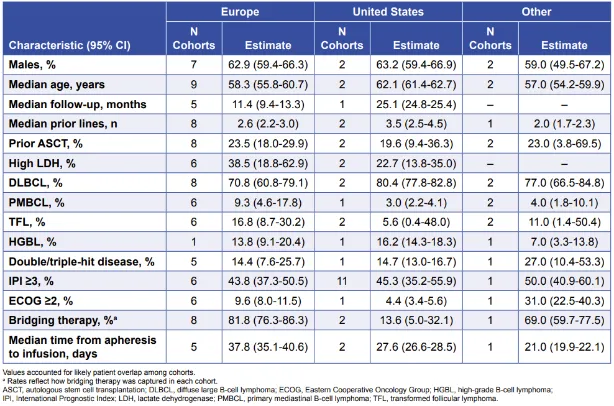
美国和欧洲队列的患者特征基本一致,但有以下例外(表1):欧洲队列的中位随访时间在数值上短于美国队列(11.4个月 vs. 25.1个月),欧洲从单采到回输的中位时间在数值上长于美国(37.8天 vs. 27.6天),但在之前报告的范围内。与Axi‑cel的临床试验相比,RWE研究中的患者群体更多来自临床晚期,其中最常见的导致不符合临床试验入组标准的因素包括桥接治疗、异基因干细胞移植和美国东部肿瘤协作组体能状态(ECOG PS)评分≥2分。
表1 患者特征的荟萃分析
估计的欧洲任何级别细胞因子释放综合征(CRS)的发生率为88%(95% CI,85%-91%),美国为82%(95% CI,81%-84%)。估计的欧洲≥3级CRS发生率为8%(95% CI,7%-10%),美国为7%(95% CI,5%-10%;图 2)。≥3级CRS的发生率从2019年12月之前队列的 11%(95% CI,7%-16%)下降到2019年12月之后队列的8%(95% CI,5%-12%)。
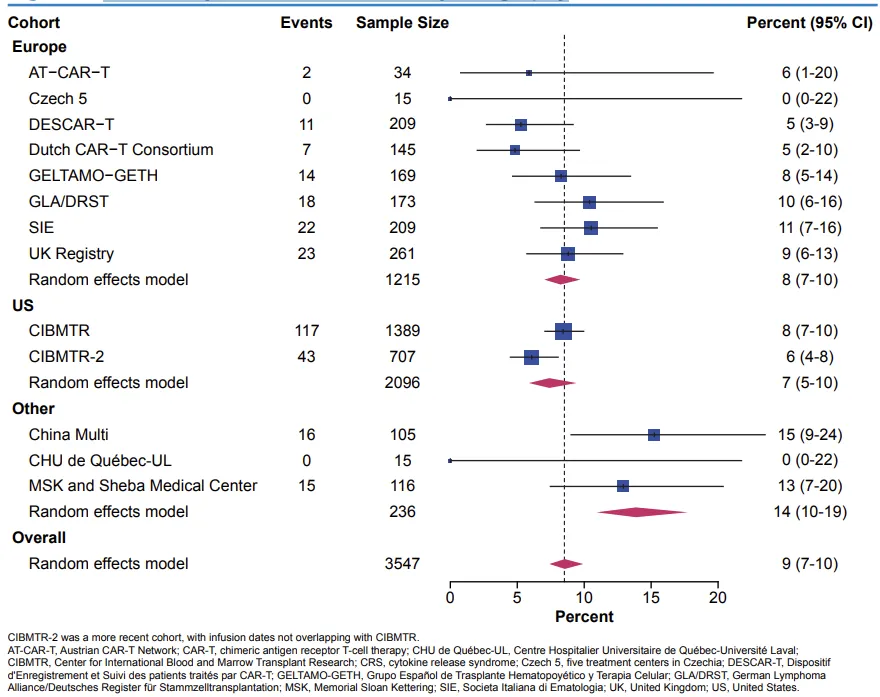
图2 按地区分层的3级及以上CRS的荟萃分析
欧洲和美国任何级别的免疫效应细胞相关神经毒性综合征(ICANS)的估计发生率分别为47%(95% CI,41%-53%)和50%(95% CI,40%-60%)。欧洲≥3级ICANS的发生率(17% [95% CI,15%-20%])数值上低于美国(24% [95% CI,20%-28%];图3),美国和欧洲≥3级ICANS的估计值均在ZUMA-1研究报告的发病率范围内。
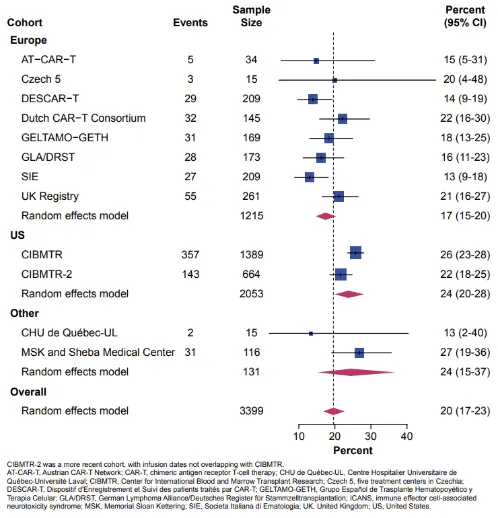
图3 按地区分层的≥3级ICANS的荟萃分析
欧洲任何级别长期
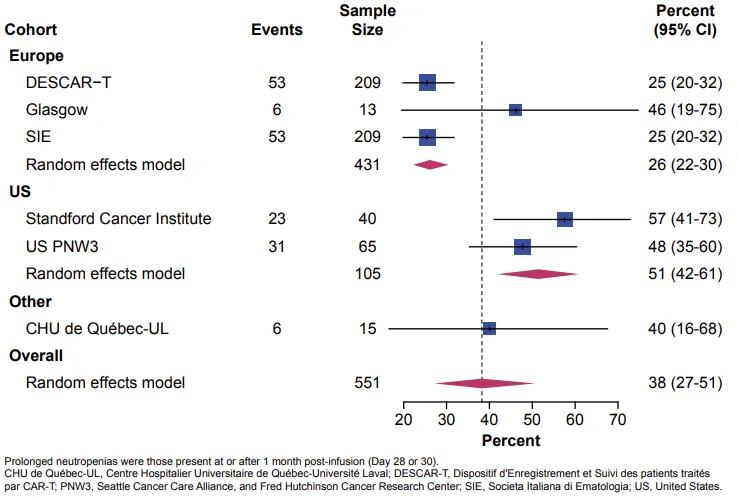
图4 按地区分层的≥3级长期中性粒细胞减少症的荟萃分析
欧洲与美国的托珠单抗使用率分别为71%(95% CI,67%-74%)vs. 58%(95% CI, 55%-61%)。欧洲类固醇激素的使用率为45%(95% CI,31-61),美国为48%(95% CI,46%-51%)(图5)。2019年12月前后队列托珠单抗使用率一致(70% [95% CI,59%-78%] vs. 72% [95% CI,61%-81%]),而类固醇激素的使用率在数值上有所增加(54% [95% CI,41%-67%] vs 67% [95% CI,56%-77%])。此外,欧洲重症监护病房入院率为20%(95% CI,14%-28%),美国重症监护病房入院率为24%(95% CI,15%-37%)。

图5 按地区分层的类固醇激素使用情况的荟萃分析
研究结论
Axi‑cel在R/R DLBCL和FL患者中的安全性RWE证据数量充足且质量稳健,欧洲证据的数量和质量比之前有了显著提高。总的来说,Axi‑cel治疗安全性可控,且在不同地区及临床试验之间保持一致,提高的安全性可能促进了真实世界中CAR-T治疗管理的演变。
免责声明:本资料为专业医学资料,旨在促进医药信息的沟通和交流,仅供医疗卫生专业人士参考;任何处方请参考产品最新详细处方资料。本文件可能包含涉及医学情况、健康及治疗方法的信息。相关信息不得用作诊断或治疗,不能替代专业医学意见。
审批编号:NP-NHL-Axi-Cel-2024.6-28 valid until 2026.6