
随着创新药物的持续发展及医疗水平的不断提高,
第21届国际骨髓瘤学会(IMS)年会于2024年9月25日-28日在巴西里约热内卢召开,会议公布了MM治疗领域最新研究摘要。本期精选了3篇有关探寻新治疗方案的研究,共享以卡非佐米为基础的新药联合方案治疗NDMM、RRMM的最新研究成果。
再传佳音:Isa‐KRd四药联合诱导方案可为NDMM患者带来较高MRD阴性率
【OA-54】适应性巩固治疗前Isa‐KRd诱导治疗适合移植NDMM患者的疗效和安全性:IFM2020‐02 MIDAS研究的中期分析
Efficacy and Safety of Isa‐KRd Induction Before Response‐Adapted Consolidation in Transplant Eligible Newly Diagnosed Multiple Myeloma: An Interim Analysis of the IFM2020‐02 MIDAS Study
研究设计:该研究旨在评估Isatuximab联合卡非佐米[首次剂量为20 mg/m2,此后(每周期第1、8、15天)剂量为56 mg/m2]、
研究结果:该研究从72家中心纳入791例患者,中位年龄约59岁。其中8%的患者仅符合SLiM标准,13%的患者分期为国际分期系统(ISS)III期,5%的患者为修订的国际分期系统(R-ISS)III期。在接受细胞遗传学评估的791例患者中,8%的患者LP评分>1,26%的患者伴t(11;14),接受PET-
所有患者均接受了Isa-KRd诱导治疗(意向治疗,ITT),其中757例患者完成了6个周期诱导治疗(符合方案集,PP),766例患者接受过≥1次PSC动员。结果CD34+细胞采集中位数为7×106/kg,共721例患者采集的PSC符合串联移植要求。
总有效率(ORR)为99%。ITT和PP人群分别有92%、99%的患者达≥非常好的部分缓解(VGPR)。在可评估的751例患者中,ITT和PP人群中分别有63%、66%的患者达MRD阴性(<10-5),分别有47%、50%的患者达MRD阴性(<10-6)(图1)。
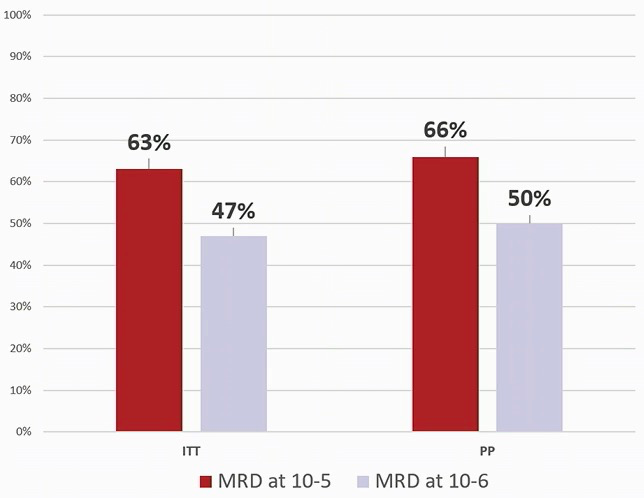
图1 不同人群的MRD阴性率
在诱导治疗期间,<1%的患者死亡。常见的3-4级AE为中性粒细胞减少(25%)、
研究结论:Isa-KRd诱导方案可为患者带来深度缓解和较高的MRD阴性率,且可成功采集PSC,治疗期间未出现新的AE。需后续随访的最终分析确认临床获益。
扬帆起航:Iber-DKd/Iber-Dd方案巩固治疗助力清除NDMM患者持续存在的MRD
【P-326】Ib/II期临床试验:采用Iber-Dd±K巩固治疗以清除NDMM诱导治疗及ASCT后持续存在的MRD
Phase 1b/2 Trial of Iberdomide in Combination with Daratumumab, Dexamethasone +/‐ Carfilzomib to Eliminate MRD After Induction Therapy and ASCT in NDMM
研究设计:Iberdomide(Iber)是新型cereblon E3泛素连接酶免疫调节剂,可与其他MM药物联合使用。该研究旨在评估Iber联合
研究结果:共纳入27例患者,中位年龄为67岁,其中7例伴有高危
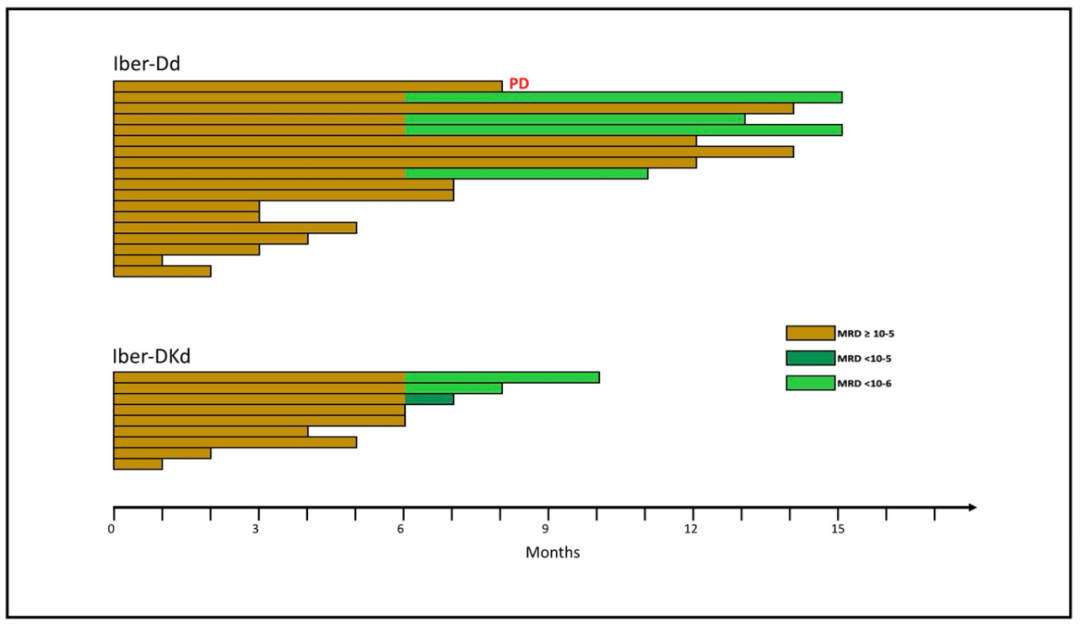
图2 不同治疗组患者在不同治疗时间的MRD水平
Iber-Dd组常见的AE为中性粒细胞减少(8/18,6例≥3级)、血小板减少症(5/18,均为1-2级)和感染(6/18,2例≥3级);Iber-DKd组常见的AE为感染(5/9,2例≥3级)。
研究结论:Iber-Dd和Iber-DKd是安全有效的联合方案,其有助于清除NDMM患者经诱导治疗和ASCT后持续存在的MRD。该研究仍在进行中。
卓有成效:BelMaf-KRd方案可助力伴有高危因素的RRMM患者获得深度缓解且安全性可控
【OA-57】BelMaf联合KRd治疗经治MM的I期临床试验结果
Results of a Phase 1 Clinical Trial of Belantamab Mafodotin (BelMaf) Combined with Carfilzomib, Lenalidomide, and Dexamethasone (KRd) for Multiple Myeloma (MM) After One Prior Line of Therapy (LOT)
研究设计:BelMaf是靶向BCMA的新型抗体-药物偶联物,该研究旨在评估BelMaf联合KRd治疗RRMM患者的有效性和安全性。为指导确定II期推荐剂量(RP2D),I期临床试验为3+3剂量递增设计,随后进行扩展队列。治疗方案为18个周期BelMaf(剂量①:1.4 mg/kg/8周,或剂量②:1.9 mg/kg/8周)-KRd(K:20或56 mg/m2,第1、8、15天;R:25 mg/天,第1-21天;d:20或40 mg/周)治疗+R维持治疗。主要终点是根据第一疗程剂量限制性毒性(DLT)确定BelMaf-KRd的最大耐受剂量(MTD)。次要终点包括ORR、VGPR率等。
研究结果:共纳入19例患者,其中6例患者接受剂量①治疗,13例患者接受剂量②治疗。患者中位年龄为63岁,47.3%的患者细胞遗传学高危(HRCG),15例患者有分期数据且33.3%的患者分期为III期。42.1%、10.5%和26.3%的患者分别对来那度胺、
中位随访11.8个月,最佳ORR为100%,≥VGPR率和≥CR率分别为58%和53%,MRD阴性率(10-5和10-6)约为70%、42%(图3)。2年PFS率和OS率分别达80%和95%。
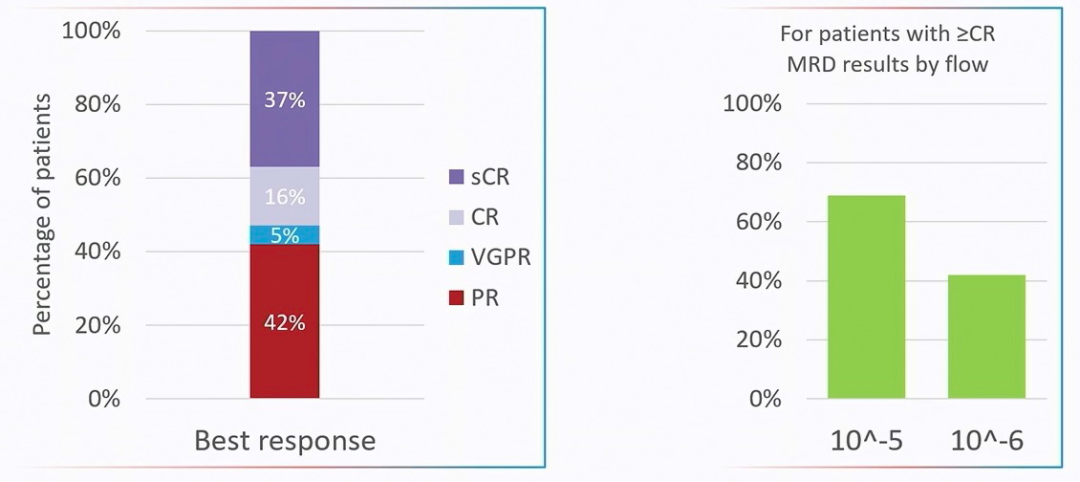
图3 患者缓解深度
常见的AE包括角膜病变(94.7%,≥3级31.6%)、
研究结论:BelMaf-KRd的MTD和RP2D均为1.9 mg/kg/8周。细胞遗传学高危和R难治患者接受BelMaf-KRd治疗后也可获得深度缓解。角膜病变可通过延长给药时间和减少剂量来控制。
教授点评
许贞书教授
随着人口老龄化加重,MM发病率持续攀升5,其诊疗相关的问题日渐突出;且MM患者面临复发率高等问题,对治疗后缓解深度发出了更高的需求。卡非佐米的出现为MM患者带来新的希望。无论患者是否适合移植,中国CSCO指南均将卡非佐米联合来那度胺、地塞米松(KRd)作为NDMM的I级推荐2。对于适合移植的NDMM患者,诱导治疗推荐使用PI联合联合免疫调节剂及地塞米松的方案,在此基础上加入新药的四药联合方案有望获得更好的诱导疗效尤其是MRD转阴率6。
MRD阴性已成为MM疗效评估的重要指标,MRD与细胞遗传学高危被视为MM的独立不良预后因素,故患者接受治疗后达到MRD阴性至关重要;今年FDA已同意将MRD阴性作为MM加速批准终点7,进一步肯定了MRD的临床价值。既往研究8表明,Isa-KRd可为NDMM患者带来较高MRD阴性率,患者在接受诱导治疗后、ASCT后和巩固治疗后的MRD阴性率分别为45%、64%和77%;同时,Isa-KRd方案可为高危患者、双打击患者带来与标危患者相当的缓解深度获益。OA-54报道的结果也证明了Isa‐KRd四药联合诱导方案可促进NDMM患者获得深度缓解。本次P-326报道亦初步证明了Iber-Dd和Iber-DKd联合方案可助力清除NDMM患者经诱导治疗和ASCT后持续存在的MRD,提高MRD转阴率,以期更长生存。
除NDMM外,以卡非佐米为基础的联合方案亦显著改善了RRMM患者的预后。ASPIRE研究4采用KRd/Rd治疗RRMM患者,结果显示,与Rd组相比,KRd组患者获益显著,ORR、≥CR率分别为87.1%、31.8%,≥VGPR率达69.9%,且安全性可控。此外,OA-57报道的以KRd为基础的新药联合方案(BelMaf-KRd)可为RRMM患者带来深度缓解,其在伴有高危因素或R难治性患者中亦展现出良好的前景。
整体来讲,卡非佐米作为MM治疗的基石性药物,未来通过持续探索其联合其他新药的疗效和安全性,以期为患者带来更多深度缓解获益,并最终转化为长期生存。