
移植物抗宿主病(GVHD)是导致异基因造血干细胞移植(allo-HSCT)后死亡率和发病率的重要因素。兔抗胸腺细胞免疫球蛋白(rATG)已被用于allo-HSCT预处理方案/预防,作为体内消耗T淋巴细胞以预防GVHD的策略,但其最佳剂量尚未确定。因此,Zuckermann J等人展开了一项系统性回顾和荟萃分析,旨在确定不同剂量rATG在allo-HSCT中的疗效和安全性,结果已在《PLoS One》杂志上发表。
01研究设计
本研究于2020年3月21日至2022年3月1日采用“骨髓移植”等关键词检索了MEDLINE/PUBMED、EMBASE、Cochrane Library、Web of Science、LILACS和SciELO数据库中的文献(无时间限制)。纳入标准:所有年龄段患者行相关(HLA匹配或半相合)或无关(HLA匹配和HLA不匹配)HSCT的比较性研究,研究中患者使用rATG(ATG-F或ATG-T)作为GVHD预防中T细胞耗竭的策略。系统性回顾和荟萃分析比较了不同剂量rATG组的结果。在语言、随访时间或日期限制方面无任何限制。最终纳入22篇文献。共有5项研究(1项随机对照试验和4项观察性研究)使用ATG-F,17项研究使用ATG-T(5项随机对照试验和12项观察性研究)。基于ATG-T和ATG-F对分析进行分层。在纳入的研究中,ATG-T的高剂量为4-12mg/kg,低剂量为2-7.5mg/kg,ATG-T在移植前的第9至第1天内给药。ATG-F的最高剂量范围>10–120mg/kg,患者在移植前第5至第1天内给药。ATG-F的低剂量范围<10-50mg/kg。
02研究结果
ATG-T的结局
高剂量ATG-T组Ⅱ-Ⅳ级aGVHD的发生率较低(RR 0.79; 95%CI: 0.66–0.95, I2=49%)(如图1a),Ⅲ-Ⅳ级aGVHD的发生率也较低(RR 0.60;95%CI: 0.41–0.87, I2=49%)(如图1b)。
高剂量ATG-T组显著降低了局限性cGVHD的风险(RR 0.64, 95%CI: 0.45–0.92, P=0.02, I2=34%)(如图1c)。广泛性cGVHD和总体cGVHD的发生率在高剂量和低剂量ATG-T组之间均无显著差异(如图1d,e)。
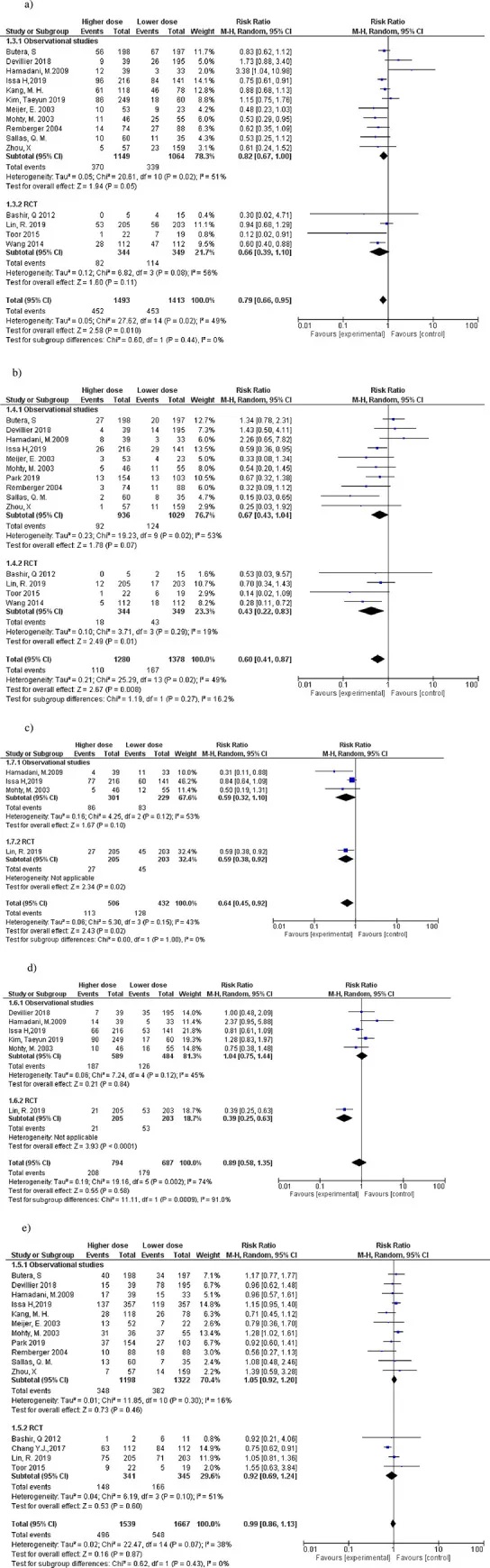
图1 比较高剂量和低剂量ATG-T组之间急性和慢性GVHD的森林图。a)Ⅱ-Ⅳ aGVHD,b)Ⅲ-Ⅳ aGVHD,c)局限性cGVHD,d)广泛性cGVHD,e)总体cGVHD
高剂量ATG-T组移植后巨细胞病毒(CMV)再激活的风险增加(RR 1.21, 95%CI: 1.05-1.39, I2=68%)(如图2a)。值得注意的是,当总结随机临床试验时,其风险降低(RR 1.10, 95%CI: 1.02-1.20, I2=0%)。高剂量ATG-T组EB病毒(EBV)再激活(或EB相关淋巴增生性疾病)风险增加(RR 1.40, 95%CI: 1.01–1.94, p<0.00001, I2=77)(如图2b)。
高剂量ATG-T组的原发性疾病复发率更高(RR 1.34, 95%CI: 1.07-1.67, I2=0%)(如图2c)。高剂量ATG-T组和低剂量ATG-T组之间移植相关死亡率无显著差异(如图3d)。共6项使用ATG-T的研究报告了植入失败(如图2e);两项研究报告了继发性失败,高剂量和低剂量ATG-T之间无差异。仅1项研究报告无植入失败事件。高剂量和低剂量ATG-T之间植入失败率无差异。
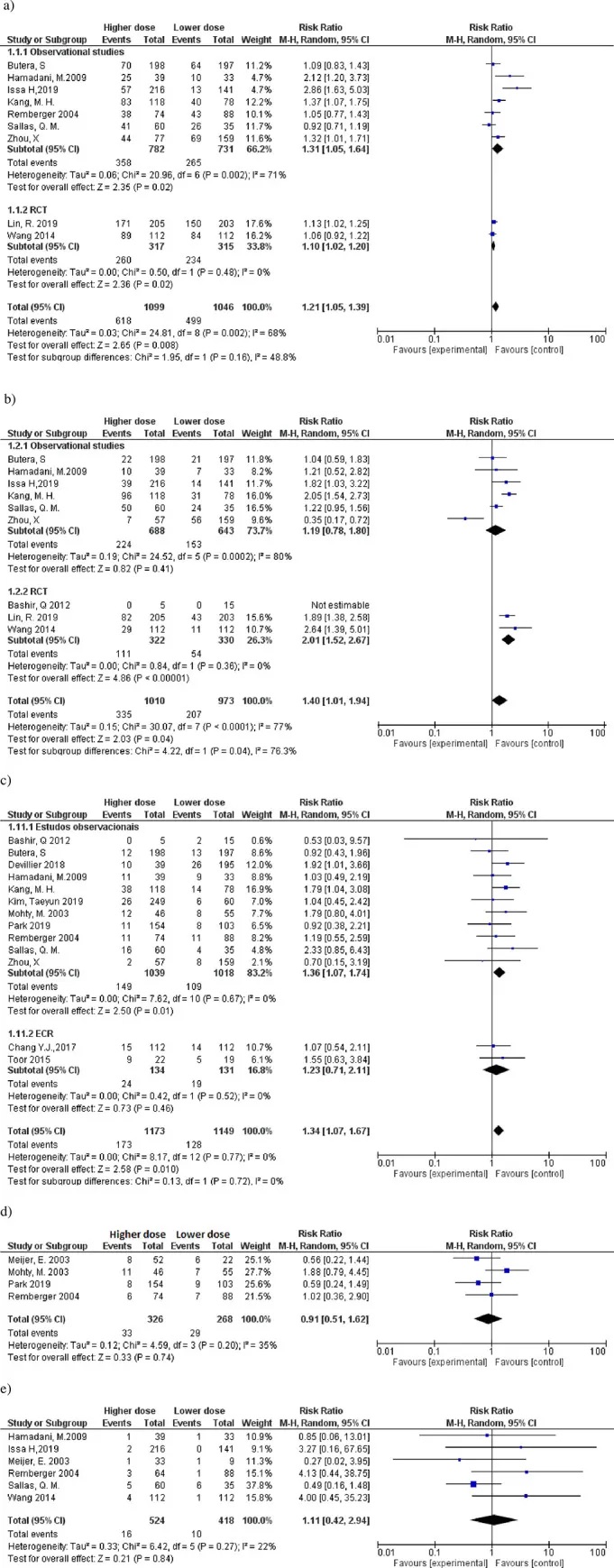
图2 比较高剂量和低剂量ATG-T组之间相关结果的森林图。a)CMV再激活,b)EBV再激活或EBV相关的淋巴增生性疾病,c)校正1年原发性疾病复发率,d)校正1年移植相关死亡率,e)原发性或继发性植入失败
敏感性分析
事后敏感性分析仅包括随机临床试验,比较接受较高ATG-T剂量≥7mg/kg组与较低剂量<7mg/kg组的结局(组间无剂量重叠)。ATG-T剂量≥7mg/kg组相较于ATG-T剂量<7mg/kg组因Ⅲ-Ⅳ级aGVHD需要治疗的患者数量为7.4个,因1年复发需要伤害的人数为7.7个。ATG-T剂量≥7mg/kg组Ⅲ-Ⅳ级aGVHD的风险降低了74%(RR 0.26, 95%CI: 0.11–0.60)(如图3a),Ⅱ-Ⅳ级aGVHD也有获益的趋势(RR 0.44, 95 CI: 0.19–1.04)(如图3b)。ATG-T剂量≥7mg/kg组1年复发风险增加了80%(RR 1.80, 95%CI: 1.13–2.89)(如图3c),EB病毒再激活或EB相关淋巴增生性疾病的风险增加了64%(RR 2.64, 95%CI: 1.39–5.01)(如图3d)。
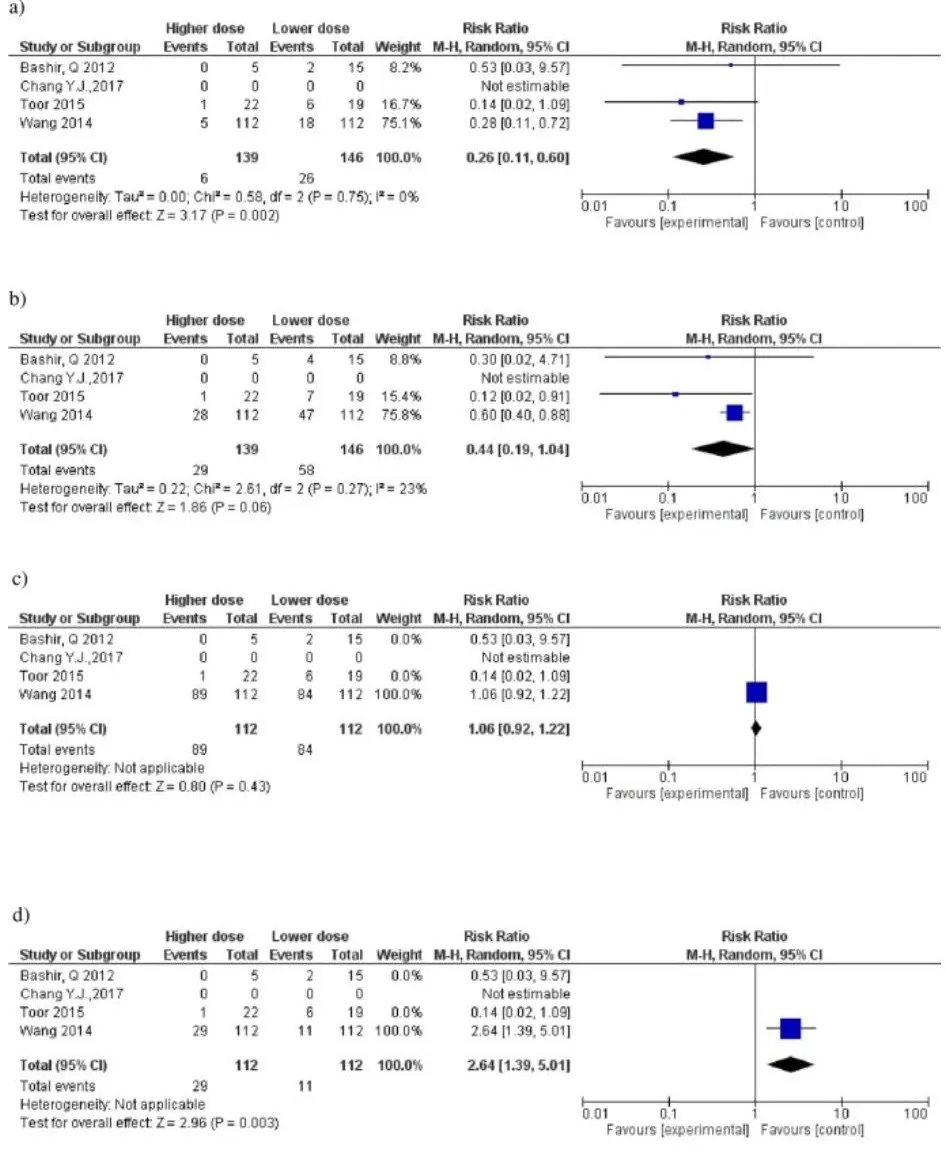
图3 ATG-T剂量<7 mg/kg与≥7mg/kg比较的森林图。a)Ⅲ-Ⅳ级aGVHD。b)Ⅱ-Ⅳ级aGVHD。c)CMV再激活。d)EBV再激活或与EBV相关的淋巴增生性疾病
对移植类型的敏感性分析显示,接受无关供者移植(HLA匹配和HLA不匹配)的患者,使用高剂量的ATG-T,II-IV级aGVHD(RR 0.71, 95%CI: 0.59-0.85, I2=0%)和III-IV级aGVHD(RR 0.52,95%CI: 0.34-0.79, I2=0%)的发生率较低。考虑到预处理方式,荟萃分析表明,更高剂量有利于接受清髓预处理的患者预防II-IV级aGVHD(RR 0.73;95%CI: 0.53–1.00, I2=45%),以及III-IV级aGVHD的发病率(RR 0.44, 95%CI: 0.24–0.83, I2=26%)。在预防aGVHD方面,接受低强度预处理(RIC)的患者的高剂量和低剂量ATG-T无差异,而在高剂量的ATG-T中,总体cGVHD的风险显著增加(RR 1.15;95%CI 1.01-1.31, I2=0%)。
基于移植类型进行的敏感性分析显示,在接受单倍型相合的造血干细胞移植患者中,高剂量组存在CMV再激活风险(RR 1.10, 95%CI: 1.0-1.21, I2=29%)。关于移植和预处理方式,清髓性预处理组患者仍存在高剂量再激活的风险(RR 1.10, 95%CI: 1.02-1.19, I2=0%),尤其是RIC组(RR 2.46;95%CI 1.65-3.68, I2=0%)
高剂量的ATG-T的清髓预处理维持了EBV发生率的最大风险(RR 2.01, 95%CI: 1.52-2.67 , I2=0%),在RIC中也呈现出风险更大的趋势(RR 1.60, 95%CI: 1-2.57, I2=0%)。高剂量的ATG-T显示RIC患者的复发和复发风险更大(RR 1.53, 95%CI: 1.05-2.23, I2=0%),而清髓预处理方案的剂量之间无差异。
考虑到ATG输注的时间,从移植前第5天到第1天首次输注ATG的亚组在高剂量ATG治疗下Ⅱ-Ⅳ和Ⅲ-Ⅳ级aGVHD均显示出较低的发病率(RR 0.39,95%CI: 0.22–0.69;RR 0.23, 95%CI: 0.10–0.51),而从移植前第9天到第6天首次输注的亚组在高剂量和低剂量之间Ⅱ-Ⅳ和Ⅲ-Ⅳ级aGVHD发病率均无差异(RR 0.74, 95%CI: 0.55–1.00;RR 0.66, 95%CI : 0.38–1.15)。
03结论
本项荟萃分析的结果显示,较高剂量ATG在预防GVHD方面具有优越性,但CMV和EBV感染和复发风险更高。然而,研究的方法学质量较低,高剂量和低剂量的定义缺乏一致性,因此无法得出风险-收益结论。需要大型且精心设计的随机对照试验来回答这一相关问题。
免责声明:该信息仅作医学和科研参考,赛诺菲不建议以任何与您所在国家所批准的处方信息不符的方式使用本产品。本材料仅供医疗卫生专业人士使用。
MAT-CN-2405806/V1.0/MAR.2024
参考文献
1.Zuckermann J, et al. PLoS One. 2023;18(4):e0284476.