
抗CD19嵌合抗原受体T细胞(CAR-T)是目前治疗复发/难治性弥漫性大B细胞淋巴瘤(DLBCL)、高级别B细胞淋巴瘤、转化型滤泡性淋巴瘤(FL)、原发性纵隔大B细胞淋巴瘤和套细胞淋巴瘤的标准治疗方案。尽管CAR-T细胞治疗对很多患者都有疗效,但在DLBCL患者中,仅有30%-40%的患者可获得长期缓解,而在复发或难治性FL患者中,仅有60%的患者可获得长期缓解。因此,对于CD19 CAR-T细胞治疗无效或治疗后复发的淋巴瘤患者来说,仍需要有效的治疗方法。
已有研究表明,对CAR-T细胞治疗无反应的患者中,肿瘤和肿瘤微环境细胞中的免疫检查点相关蛋白(PD-L1、LAG3)的表达基线水平较高。临床上,已观察到有一部分进展性淋巴瘤患者在CAR-T细胞治疗后对免疫检查点阻断剂有反应。帕博利珠单抗是一种新型人源化单抗,通过与程序性细胞死亡受体1(PD-1)结合,阻断PD-1通路介导的免疫抑制反应,发挥肿瘤免疫作用。基于此,研究者展开了一项单中心、1/2a期的前瞻性研究,将帕博利珠单抗用于治疗CD19 CAR-T细胞治疗后复发/难治性B细胞淋巴瘤患者,探究帕博利珠单抗的临床疗效。
研究方法
该研究共纳入2016年6月1日至2018年6月4日期间接受CAR-T细胞治疗后复发/难治性B细胞淋巴瘤患者12例。符合条件的患者:红细胞输注时间>7天,且血小板计数≥50000/µL、绝对中性粒细胞计数≥1000/µL以及血红蛋白≥8g/dL。
入组患者每3周接受1次200mg IV的帕博利珠单抗治疗,持续1年或直至疾病进展、达到治疗限制性毒性或选择性方案终止。若患者已接受至少8次帕博利珠单抗治疗,并且在记录完全缓解(CR)后至少完成两个周期治疗,则达到CR的患者可停止治疗。帕博利珠单抗治疗前、首次使用帕博利珠单抗输注后24-72h(第1周到第6周,每周收集)、每个帕博利珠单抗治疗疗程开始前以及治疗结束后,分别收集患者外周血单核细胞(PBMCs)以及血清。
主要终点为安全性,次要终点包括临床结果(最佳总缓解率[ORR]、3个月ORR、无进展生存期[PFS]以及总生存期[OS]),以及T细胞生物学相关研究。
研究结果
入组患者特征
入组患者中有11例DLBCL患者,1例1-2级FL患者,详细患者特征见表1。12例患者中有10例患者(83%)在CAR-T细胞治疗后出现活检证实的淋巴瘤,所有患者均在CAR-T细胞治疗后显示出PET/CT可测量的疾病且Deauville评分>4。9例患者(75%)对CAR-T细胞治疗表现出难治性,3例患者(25%)在CAR-T细胞治疗后复发。
表1 患者特征
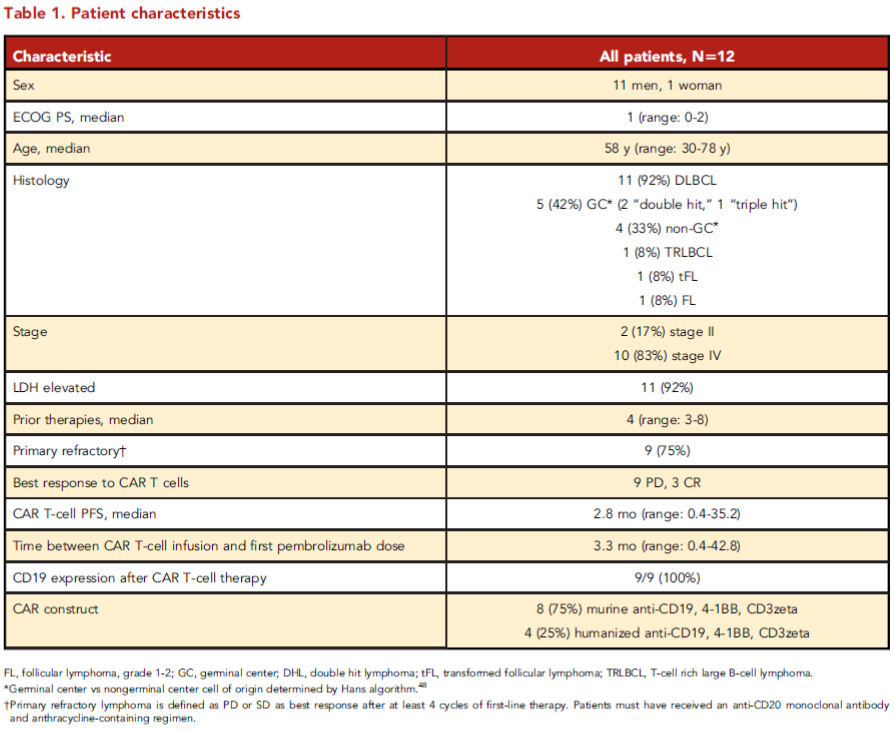
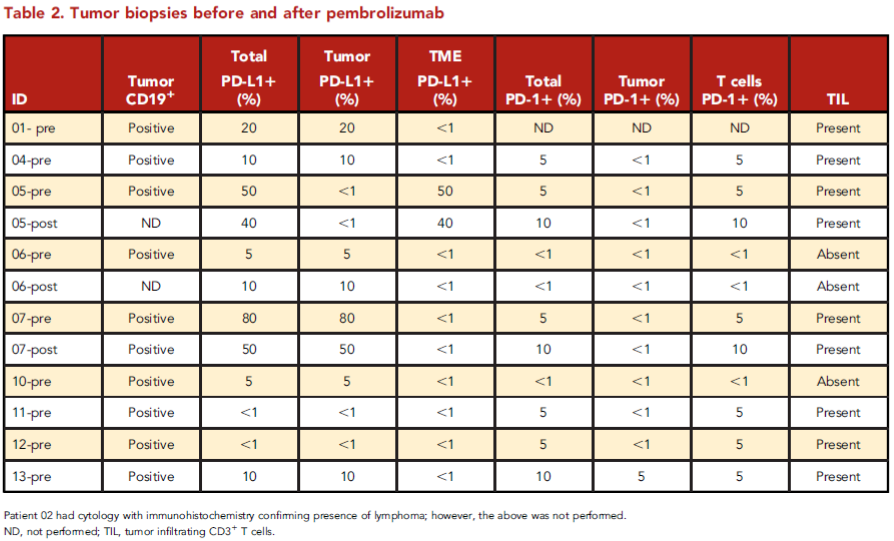
对于所有患者,CAR-T细胞治疗后的中位PFS为2.8个月(范围:0.4-35.2个月),CAR-T细胞输注到第一次帕博利珠单抗治疗的中位时间为3.3个月(范围:0.4-42.8个月)。对CAR-T细胞治疗难治性的患者,CAR-T细胞治疗后的中位PFS为2.7个月(范围:0.4-4.5个月),首次接受帕博利珠单抗治疗的中位时间为3.2个月(范围:0.4-4.6个月)。对CAR-T细胞治疗后复发的患者,CAR-T细胞治疗后的中位PFS为26.2个月(范围:19.0-35.2个月),首次接受帕博利珠单抗治疗的中位时间为27.1个月(范围:20.2-42.8个月)。帕博利珠单抗治疗的中位剂量数为2(范围:1-9)。在帕博利珠单抗治疗前,有9例患者在CAR-T细胞治疗后活检检测CD19,7/9例患者的免疫组化结果显示PD-L1的表达量达到了5%以上,见表2。12例患者中有10例未接受任何皮质醇治疗,且无患者在帕博利珠单抗相近时间接受托珠单抗治疗。在接受鼠源和人源CAR-T细胞治疗的患者中,帕博利珠单抗治疗后的安全性与有效性无差异。
表2 帕博利珠单抗治疗前后的肿瘤组织活检
安全性
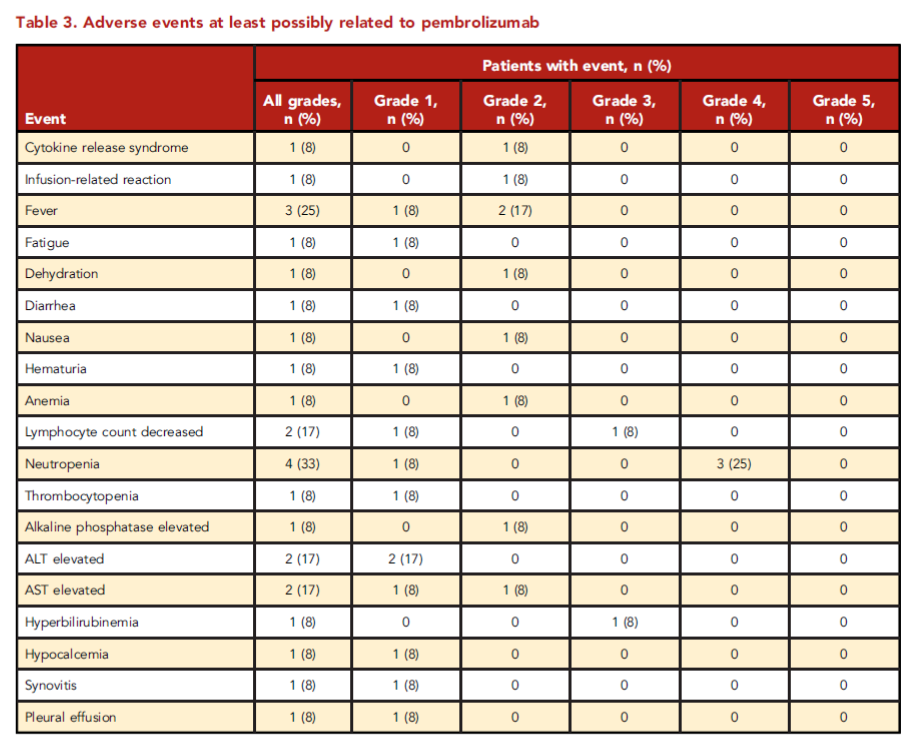
帕博利珠单抗的耐受性普遍良好,患者在治疗过程中出现的与帕博利珠单抗相关的不良事件详见表3。中性粒细胞减少是最常见的3-4级不良事件(n=3,25%),但可通过粒细胞集落刺激因子缓解。中性粒细胞减少的患者中性粒细胞增长后,在帕博利珠单抗后出现了中性粒细胞减少的复发。无发热性中性粒细胞减少症的发生。3例患者(25%)在首次输注帕博利珠单抗后出现1-2级发热。1例患者在第一次帕博利珠单抗输注10min后以及CAR-T细胞输注96天后,出现2级输注相关反应。该患者在首次帕博利珠单抗输注1天后出现2级细胞因子释放综合征(CRS),并给予支持治疗。同时还观察到了转氨酶升高(n=2,17%)、滑膜炎(n=1,8%)、血尿(n=1,8%)、胸腔积液(n=1,8%),均经帕博利珠单抗治疗后缓解。1例患者(8%)出现1级疲劳。1例患者出现3级高胆红素血症(可能与帕博利珠单抗相关)后发现有巨细胞病毒(CMV)感染(与帕博利珠单抗无关,4级),最终导致治疗方案终止。
表3 与帕博利珠单抗有关的不良事件
疗效
共评估了12例患者的临床反应,帕博利珠单抗治疗后的最佳ORR为25%(1例CR,2例部分缓解[PR])(图1)。3个月ORR为25%(1例CR,2例PR)。3个月临床获益率为33%(1例CR,2例PR,1例疾病稳定[SD])。FL患者对帕博利珠单抗无反应。9例CAR-T细胞治疗难治性患者中有2例(22%)对帕博利珠单抗有反应,3例(33%)CAR-T细胞治疗后复发的患者中有1例对帕博利珠单抗有反应。8例患者在接受帕博利珠单抗治疗时有疾病进展(PD)。1例患者有假性进展。1例患者在首次使用帕博利珠单抗后2个月肿瘤增大,但活检结果显示肿瘤主要由T细胞构成,继续治疗后达到PR。所有应答患者活检结果中,均有CD3+肿瘤浸润淋巴细胞,PD-L1总表达量在10%-50%之间(表2)。4例临床受益患者中有1例患者PD-1表达量≥5%(表2)。
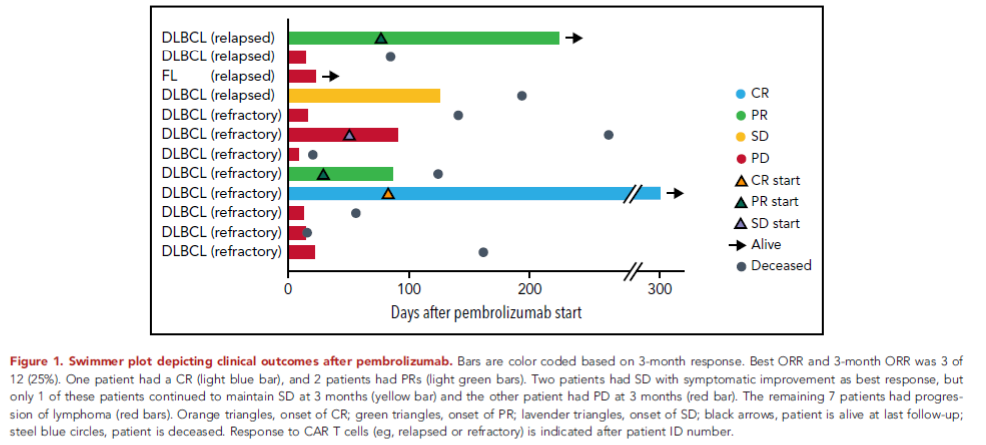
图1 帕博利珠单抗治疗前后的临床结果
帕博利珠单抗对抗CD19 CAR-T细胞的影响
12例患者中有10例患者在接受帕博利珠单抗治疗后,外周血中的CAR-T细胞再次扩增,达到CR的患者出现CAR-T细胞多次再扩增。在临床获益的患者中,帕博利珠单抗治疗后CAR-T细胞有增加趋势,帕博利珠单抗治疗无应答患者的CAR-T细胞比例在帕博利珠单抗治疗后保持稳定或下降。
通过对比对CAR-T细胞治疗应答者和无应答者的治疗前后的样本,发现在CAR-T细胞治疗后,对CAR-T细胞治疗有应答的患者,在帕博利珠单抗治疗后CAR-T细胞的激活和增殖增加,衰竭标志物减少。与无应答以及有应答的患者的非CAR-T细胞之间存在潜在差异。
研究结论
该研究证实,在CAR-T细胞输注后0.4个月使用帕博利珠单抗治疗是安全的,且耐受性良好。对CAR-T细胞治疗有应答与无应答患着在细胞生物学上存在潜在差异,这种差异影响了PD-1阻断的临床疗效。
参考来源:
Elise A. Chong, Cécile Alanio, Jakub Svoboda, et al. Pembrolizumab for B-cell lymphomas relapsing after or refractory to CD19-directed CAR T-cell therapy. Blood 2022; 139 (7): 1026–1038. doi: https://doi.org/10.1182/blood.2021012634.