
复发性或难治性B细胞急性淋巴细胞白血病(R/R B-ALL)儿童和年轻成人患者随着挽救治疗线数的增加,复发风险也相应增加。Tisagenlecleucel是一种靶向CD19的嵌合抗原受体(CAR)-T细胞疗法,已获批用于儿童和年轻成人R/R B-ALL以及成人R/R弥漫性大B细胞淋巴瘤(R/R DLBCL)和R/R滤泡性淋巴瘤(R/R FL)。II期ELIANA试验的初步结果显示,Tisagenlecleucel在R/R B-ALL儿童和年轻成人中的总有效率(ORR)达81%。此外,大多数不良事件(AE)发生在输注后的前8周,患者的生活质量(QOL)显著改善。研究者近期报道了ELIANA试验的3年随访数据。
研究方法
ELIANA是一项在R/R B-ALL儿童和年轻成人患者中开展的关于Tisagenlecleucel应用疗效及安全性的关键、II期、开放标签、多中心、全球研究。从输注Tisagenlecleucel至数据截止日期的中位时间为38.8个月。
研究结果
患者基线特征
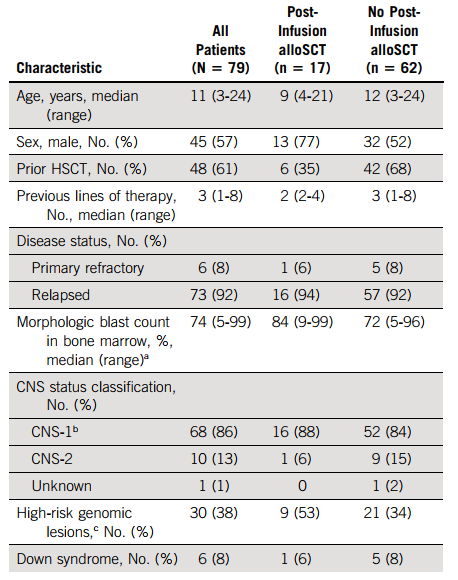
2015年04月08日至2019年07月01日,入组了97例患者,79例(81%)接受了Tisagenlecleucel治疗,包括既往报告的主要分析后的5例额外入组。患者人口统计学和临床特征详见表1。
表1:患者人口统计学和临床特征
患者疗效
前期已经发表的结果(N=75;中位随访时间为13.1个月)显示,患者的ORR为81%(95%CI,71-89%)。此次更新分析结果(N=79;从输注日期至数据截止日期的中位随访时间为38.8个月)显示,患者3个月内的ORR为82%(95%CI,72-90%)。66例达到完全缓解/完全缓解伴血液学不完全恢复(CR/CRi)的患者中位缓解持续时间(DOR)尚未达到(图1A)。患者24个月和36个月时预估的无复发生存(RFS)率分别为58%(95%CI,43-70%)和52%(95%CI,37-66%);患者24个月及36个月时预估的无删失RFS率分别为52.3%(95%CI,39-64%)和47.8%(95%CI,34.4%-60%)。在CR期间未接受后续治疗的患者(N=32)中,预估的24个月和36个月RFS率分别为81%(95%CI,62-91%)和76%(95%CI,56-88%)。
所有输注患者的中位无事件生存期(EFS)为24个月(95%CI,9.2个月至未达到;图1B),应答者(N=66)的中位EFS尚未达到(95%CI,18.7个月至未达到)。36个月时,所有输注患者的预估EFS率为44%(95%CI,31-57个月)。所有输注患者的中位总生存期(OS)尚未达到,36个月时预估的OS率为63%(95%CI,51-73%;图1C)。
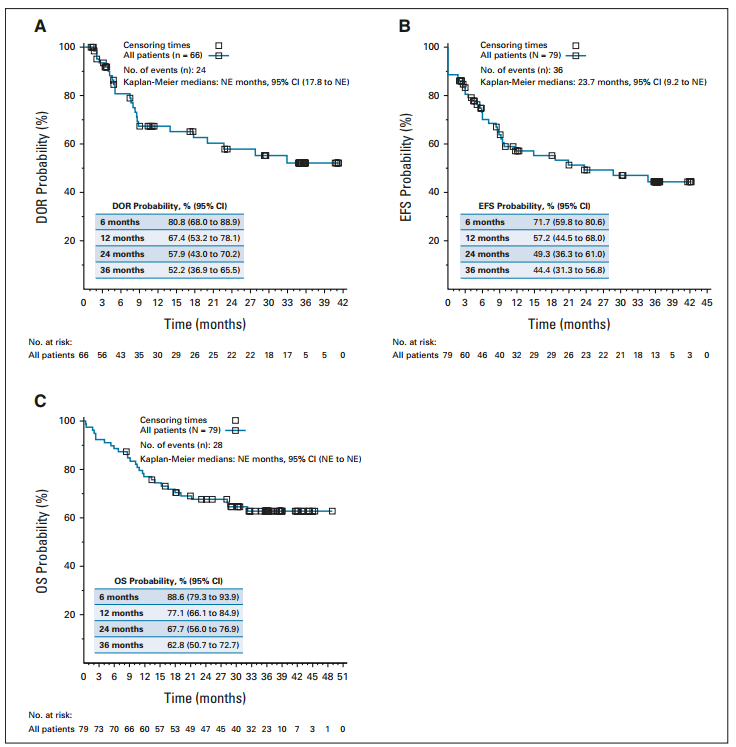
图1:该研究患者的A)DOR、B)EFS和C)OS情况
B细胞恢复的情况
应答者中至B细胞恢复的中位时间为35.3个月(95%CI,22.9%-无法估计),输注后12个月和24个月时持续性B细胞再生障碍的概率分别为71%(95%CI,57.4-81.5%)和59%(95%CI,43.2-71.2%)。在持续性B细胞再生障碍性贫血患者中,中位DOR为28个月(N=50;图2)。
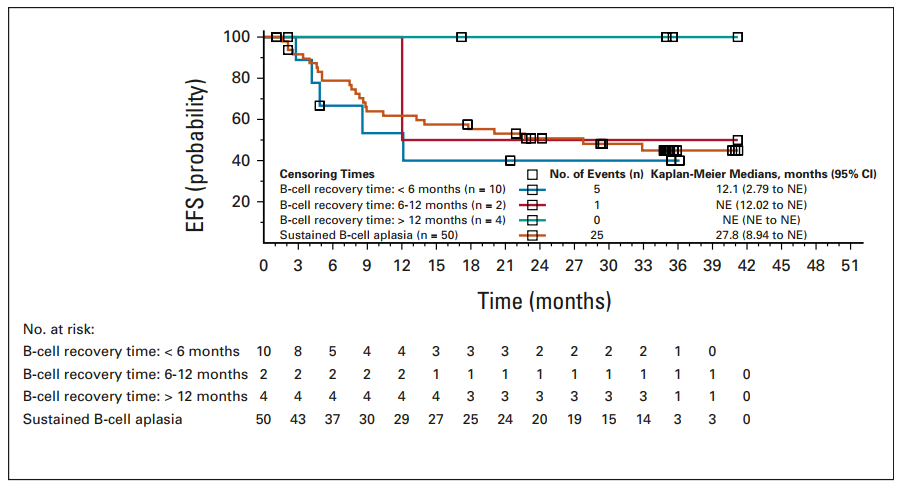
图2:按B细胞恢复时间点总结的缓解持续时间
安全性
在该长期随访分析中观察到的Tisagenlecleucel安全性特征与已发表的报告一致,未观察到新的AE或治疗相关死亡。发生3/4级AE的患者比例随时间推移而下降。输注后1年后最常见的3或4级AE为感染(20.4%)和皮肤疾病(6.1%;均为3级)。46例应答患者在基线和至少一次基线后访视时接受了儿科生活质量量表和欧洲生活质量-5维问卷视觉模拟量表(EQ-5D VAS)评估。输注后3个月健康相关QOL的临床意义有改善,在随后的36个月内持续得到改善。
研究结论
ELIANA试验3年更新结果证明了Tisagenlecleucel可作为既往接受过多线治疗的儿童和年轻成人R/R B-ALL患者的治疗选择,且长期安全性良好。