
嵌合抗原受体T(CAR-T)细胞是复发/难治性(R/R)B细胞淋巴瘤和急性淋巴细胞白血病患者的有效治疗选择,目前也用于R/R多发性骨髓瘤(MM)患者的治疗。Timothy J. Voorhees等人最近评估了CD30 CAR-T疗法在一组经过多线既往治疗的R/R经典型霍奇金淋巴瘤(cHL)患者中的疗效。在这项多中心1/2期研究中,患者在用苯达莫司汀或苯达莫司汀和氟达拉滨或环磷酰胺和氟达拉滨进行淋巴细胞清除性化疗后,接受剂量递增的CD30 CAR-T细胞治疗,在可评估患者中,客观缓解率(ORR)为62%,完全缓解(CR)率为51%,1年无进展生存(PFS)率为36%。尽管临床反应率较高,但在一部分患者中观察到复发和进展。目前仍不能确定CD30 CAR-T治疗R/R cHL患者的缓解情况和缓解持续时间能否被预测。因此,目前需要进行研究来评估影响CD30 CAR-T细胞治疗反应的变量。
靶向CD19 CAR-T细胞已在弥漫性大B细胞淋巴瘤(DLBCL)和其他侵袭性B细胞淋巴瘤中得到更广泛的研究。最近的几项研究已经探索了可能与CD19 CAR-T治疗后ORR和PFS相关的临床和相关因素。在评估影响CD19 CAR-T治疗反应的因素方面,体积肿瘤负荷是一个积极研究的领域。在关键的ZUMA-1试验中,大包块疾病(>10cm)的存在与无统计学意义的较低ORR相关。然而,考虑到测量淋巴瘤直径乘积(SPD)总和的方法来评估肿瘤体积的局限性,已经评估了包括功能成像模式在内的其他方法。近期,多项研究探索了CD19 CAR-T细胞疗法治疗DLBCL之前,通过18F-氟脱氧葡萄糖(18F-FDG)正电子发射断层扫描(PET)/计算机断层扫描(CT)评估的基线代谢肿瘤体积(MTV)预测PFS和总生存期(OS)的情况。关于确定低MTV和高MTV的适当阈值仍然存在争议,目前没有公认的标准值。阈值可能需要根据淋巴瘤亚型和/或治疗阶段进行调整。对于cHL,MTV的阈值从8-225mL不等,具体取决于分析的临床环境(初始诊断、自体造血干细胞移植前状态和疾病复发)。
Timothy J. Voorhees等人进行了一项1/2期临床试验,评估了接受CD30 CAR-T细胞治疗的R/R cHL患者的单个中心队列的数据,以确定与PFS改善相关的变量。
研究方法
入组患者
该分析纳入了在2016年8月至2020年6月期间在北卡罗来纳大学(UNC)接受淋巴细胞清除性化疗后进行自体CD30 CAR-T细胞治疗的患者。入组资格包括在淋巴细胞清除性化疗和CD30 CAR-T给药时患有CD30阳性淋巴瘤的患者。桥接化疗是允许的,但不是必需的。通过桥接疗法达到CR的患者允许接受CD30 CAR-T细胞,并被纳入该分析。
最初接受治疗的8例患者的淋巴细胞清除化疗方案包括苯达莫司汀90mg/m2/天×3天,然后其余19例患者改为苯达莫司汀70mg/m2/天联合氟达拉滨30mg/m2/天×3天。在前3例成人和儿童患者中使用CAR-T的剂量为1×108CAR-T/m2,然后在其余患者中使用的剂量为2×108CAR-T/m2。
本文报告了截至2020年6月在UNC接受CD30 CAR-T治疗的所有R/R cHL患者,包括UNC队列既往发表的25例患者的更新结果和既往未发表的另外2例患者的相关数据。
临床反应和复发评估
使用Lugano标准在CAR-T细胞治疗后6周通过PET/CT成像确定疾病反应。PFS定义为从CD30 CAR-T输注到复发、进展或死亡的时间。未发生事件的患者在最后一次随访日期或截止日期(2020年11月1日)进行审查。
MTV测量
所有患者在淋巴细胞清除性化疗和CD30 CAR-T细胞输注前均进行了基线18F-FDG PET/CT扫描。在桥接治疗前接受18F-FDG PET/CT检查的患者中,评估这些扫描的MTV以提供桥接治疗前后的肿瘤负荷比较。
研究结果
患者特征
2016年8月至2020年6月期间,UNC共有27例R/R cHL患者接受了CD30 CAR-T细胞治疗(表1)。入组时,患者的中位年龄为33岁(范围:15-67岁)。男性患者18例(67%),具有结节硬化型组织学患者18例(67%),在诊断时患有III/IV期疾病患者18例(67%)。患者既往接受了中位8线治疗(范围:3-23)。在接受治疗的患者中,81%(n=22)的患者在既往接受自体造血干细胞移植后进展,37%(n=10)的患者在异基因造血干细胞移植后进展。
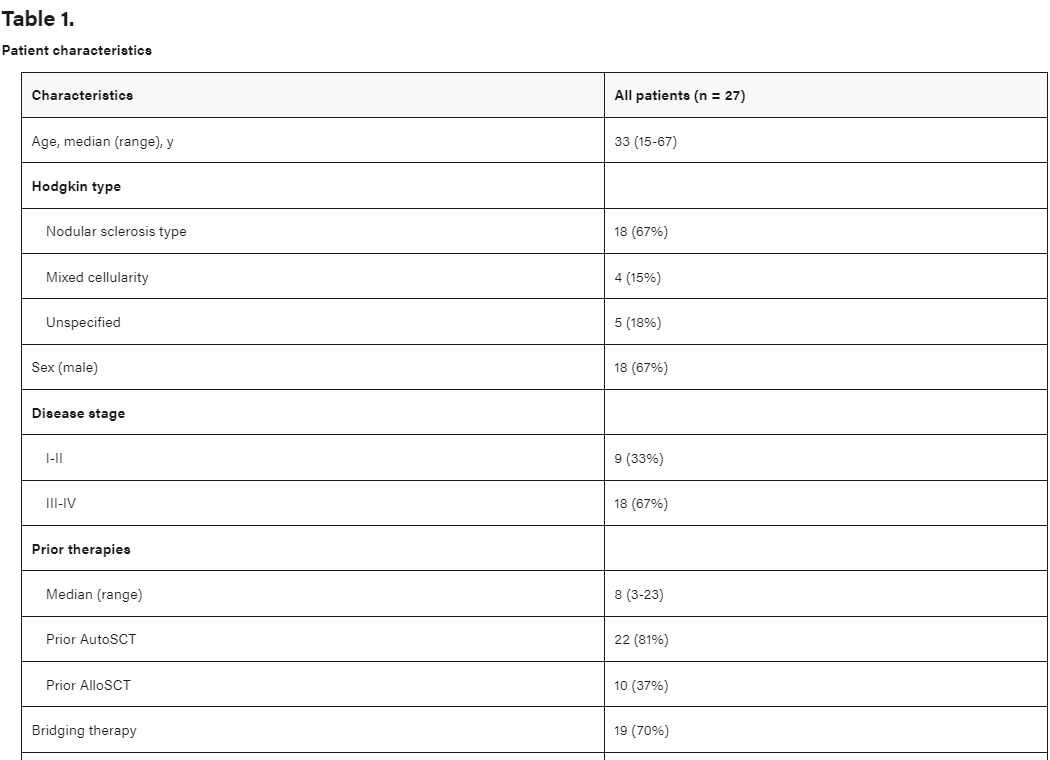
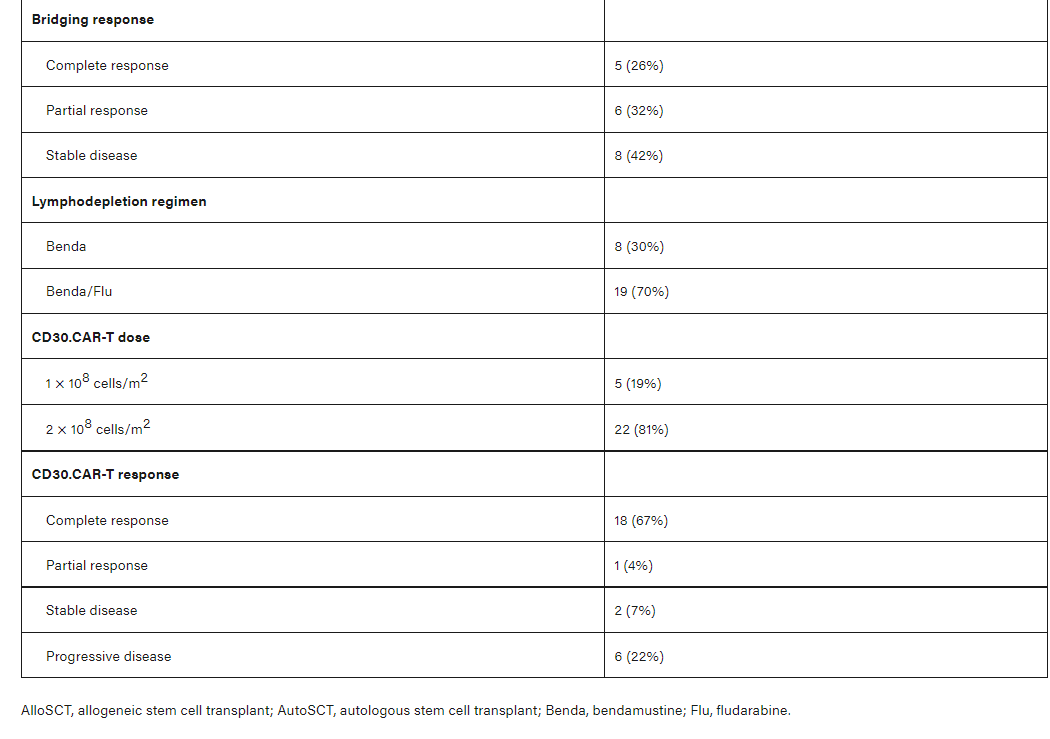
表1
桥接疗法、淋巴细胞清除性化疗和CD30 CAR-T细胞的治疗情况
该队列中有70%(19例)的患者在CAR-T细胞制备血液采集和淋巴细胞清除性化疗之间接受了桥接治疗(表1)。桥接治疗药物包括:苯达莫司汀(n=8)、苯达莫司汀加依维莫司(n=1)、苯达莫司汀加纳武利尤单抗(n=1)、抗PD-1单克隆抗体(纳武利尤单抗或帕博丽珠单抗,n=4),其他挽救化疗(n=3)、依维莫司(n=1)或维布妥昔单抗(n=1)。2例患者在全身治疗的同时接受局部放射治疗。桥接治疗的ORR为58%,其中5例患者(26%)达到CR。通过桥接治疗达到CR的患者仍然可以接受淋巴细胞清除性化疗和CD30 CAR-T细胞治疗。
所有接受CD30 CAR-T细胞治疗的患者都进行了淋巴细胞清除性化疗。前8例(30%)患者接受了苯达莫司汀,其余19例(70%)患者接受了苯达莫司汀联合氟达拉滨的淋巴细胞清除性化疗方案。
5例患者(19%)以1×108/m2的剂量接受CD30 CAR-T细胞治疗,其余22例患者(81%)的治疗剂量为2×108/m2。在CD30 CAR-T细胞输注后,6周时的ORR为71%,其中18例患者(67%)达到CR。两例患者疾病稳定(SD)并随后进展,6例患者(22%)疾病进展(PD)。总体而言,中位随访9.5个月,该队列中的17例患者(63%)出现进展,中位PFS为352天(95% CI:116-未达到),2例患者(7%)死亡,中位OS未达到(图1)。
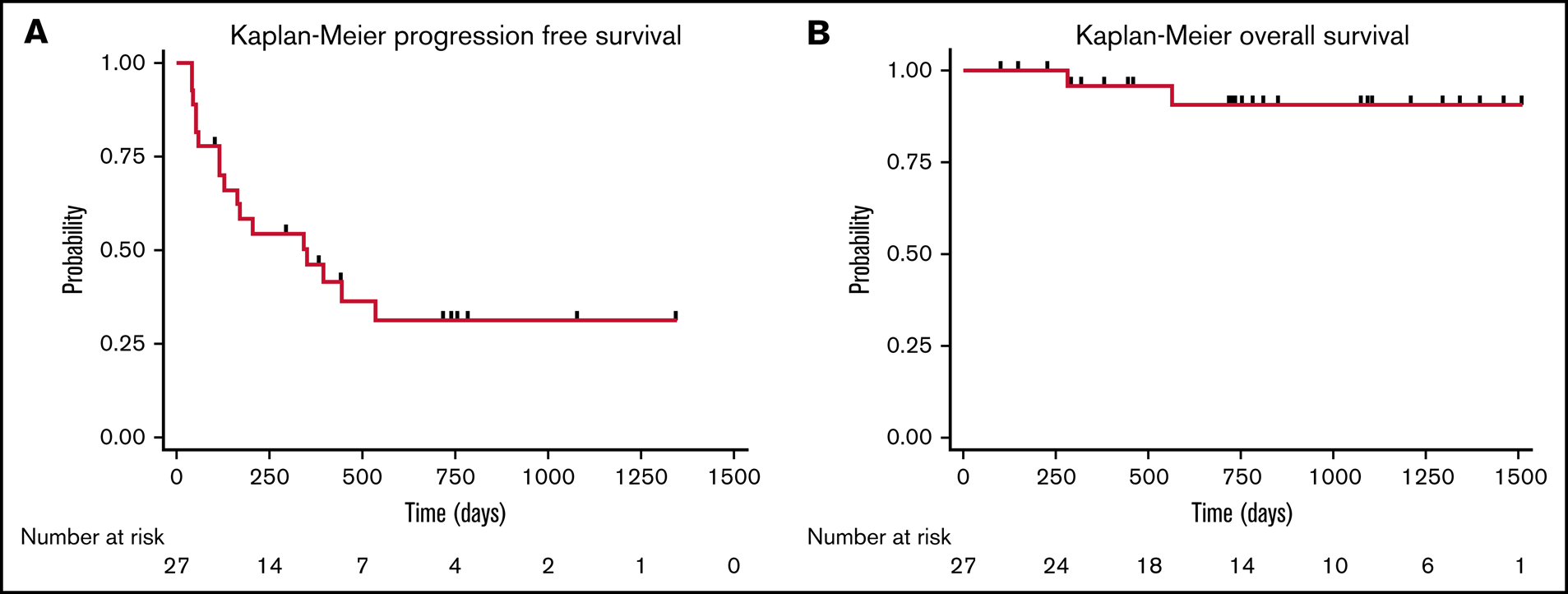
图1
MTV对PFS的影响
从18F-FDG PET/CT扫描到CD30 CAR-T细胞输注的中位时间为12天(范围:4-35天)。通过双重交叉验证分析,评估在桥接治疗后(如果适用)和淋巴细胞清除性化疗和CD30 CAR-T细胞输注之前获得的18F-FDG PET/CT扫描计算的MTV。结果显示CAR-T输注前高MTV患者具有PFS较差的趋势(P=0.07;表2)。调整淋巴细胞清除化疗后,CAR-T前高MTV与较差的PFS相关(P=0.03)。以60mL为临界值分析CAR-T前MTV显示,在未经调整的模型中以及在调整淋巴细胞清除化疗和CAR-T剂量后,高MTV>60mL与较差的PFS相关(P=0.02、0.01和0.006;图2A)。高和低基线MTV组的1年PFS率估计值分别为14%(95% CI:1%-46%)和58%(95% CI:33%-76%)。
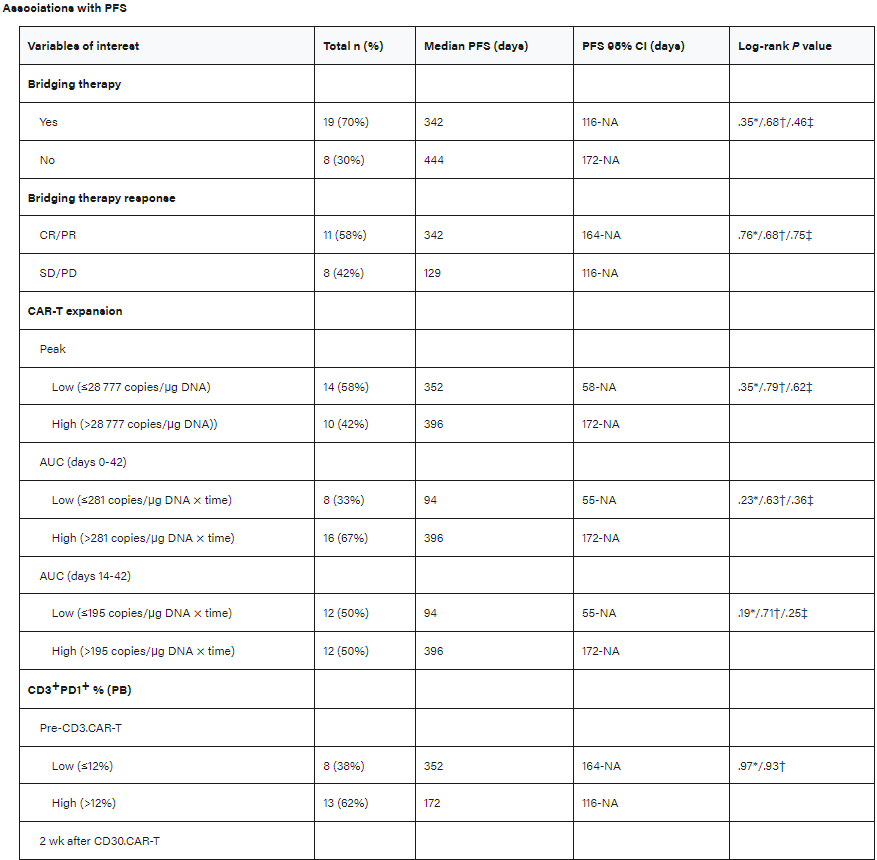
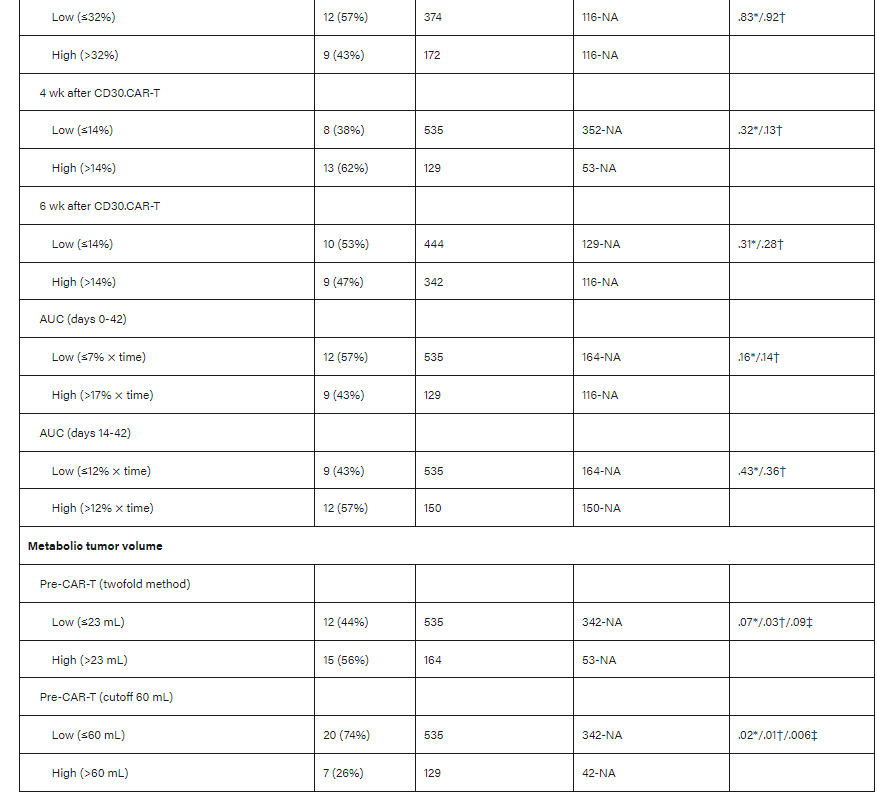
表2
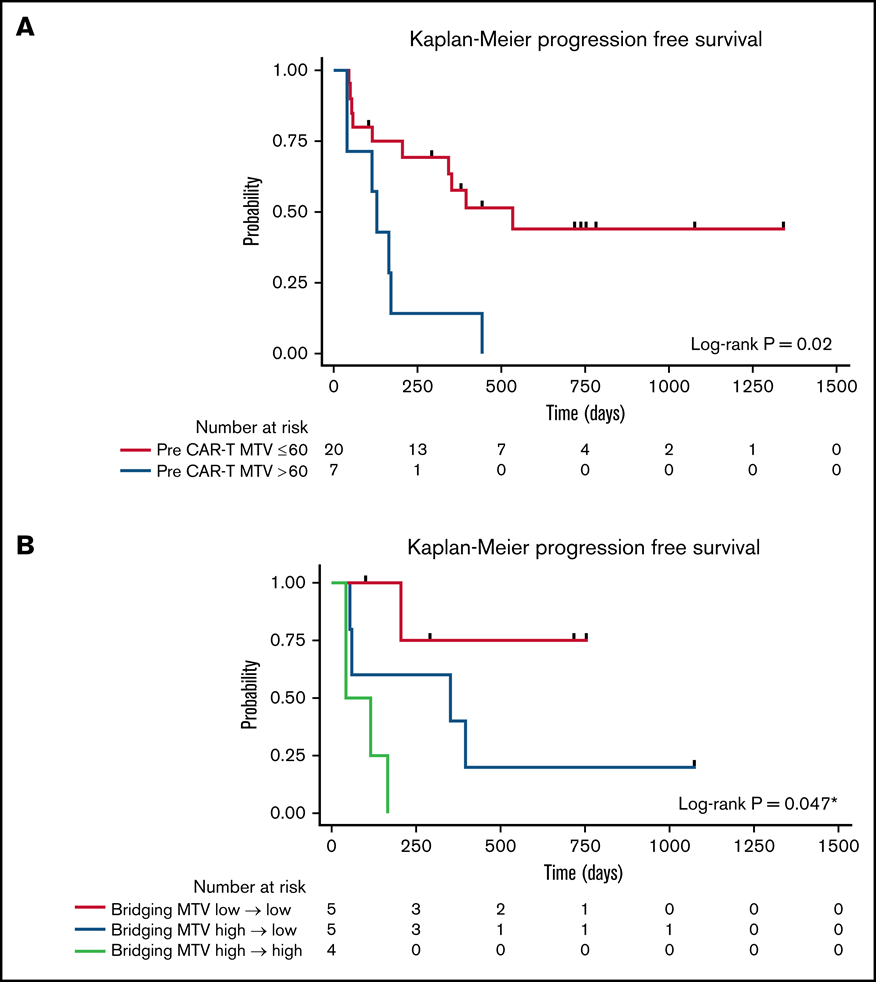
图2
研究者还评估了桥接疗法对CD30 CAR-T细胞输注后MTV和PFS的影响。桥接治疗前MTV低(≤60mL)且CD30 CAR-T细胞输注前MTV持续低的患者PFS最好(1年PFS率:75%;95% CI:13%-96%)。在CD30 CAR-T细胞输注前通过桥接治疗使高MTV(>60mL)改善至低MTV的患者具有中等PFS(1年PFS率:40%;95% CI:5%-75%)。最后,高MTV患者在桥接治疗后未改善至低MTV的患者PFS较差(1年PFS率:0%;P=0.047;图2B)。
桥接疗法、CD30 CAR-T扩增和PD-1表达对PFS的影响
接受桥接治疗的70%患者和未接受桥接治疗的30%患者的未调整估计PFS没有差异(P=0.35;表2)。此外,CD30 CAR-T扩增峰值与该队列的PFS差异无关(P=035;表2),从细胞输注(第0天)到第42天,CD30 CAR-T扩增的AUC与PFS的差异无关(P=00.23)。在CD30 CAR-T输注前评估外周血中表达PD-1的CD3+淋巴细胞的百分比,然后在输注后每周评估一次,最多6周。CD30 CAR-T输注前或CD30 CAR-T输注后PD-1表达与PFS差异无关(表2)。
研究结论
本研究报告了淋巴细胞清除性化疗与CD30 CAR-T细胞输注前,高基线MTV与R/R cHL患者更差的PFS之间的关联。结果证明,淋巴细胞清除性化疗和CD30 CAR-T细胞输注前的高MTV与较短的PFS相关,且治疗前高MTV与CD30 CAR-T输注后高循环CD3+PD-1+T细胞相关。