
第20届国际骨髓瘤学会年会(IMS)将于2023年9月27日-30日在希腊召开。双特异性抗体(BsAb)近年来逐渐成为多发性骨髓瘤的临床研究及实践的热点。本次IMS会议中公布了骨髓瘤双特异性抗体研究数据和临床管理相关更新,医脉通带您抢先了解相关研究亮点!
双特异性抗体研究数据
[P-294] 来自LocoMMotion研究和LocoMMotion + MoMMent研究的外部对照研究1:Teclistamab可显著改善三类药物暴露(TCE)的复发难治性MM(RRMM)患者的生存结局
Teclistamab是首个获批治疗TCE RRMM的基于体重、灵活给药的BCMA×CD3双特异性抗体。在I/II期MajesTEC-1研究中,Teclistamab显示出良好疗效。本研究将单臂研究MajesTEC-1中接受II期推荐剂量(RP2D剂量)(1.5 mg/kg)Teclistamab治疗的患者(N=165)与来自真实世界、前瞻性、非干预性研究LocoMMotion研究的外部对照组(N=248)或来自汇总LocoMMotion + MoMMent研究的外部对照组(N=302)进行比较。
相较于LocoMMotion研究和LocoMMotion + MoMMent研究中真实世界常用方案,接受Teclistamab治疗患者的临床获益显著改善(图1,图2)。Teclistamab vs LocoMMotion vs LocoMMotion + MoMMent:ORR(63% vs 27% vs 26%),≥CR率(46% vs 0.4% vs 0.3%),中位DOR(21.6个月 vs 7.3个月 vs 8.1个月),中位PFS(11.3个月 vs 4.1个月 vs 4.1个月),中位OS(21.9个月 vs 11.8个月 vs 13.3个月)。

图1 Teclistamab vs LocoMMotion vs LocoMMotion+MoMMent缓解率
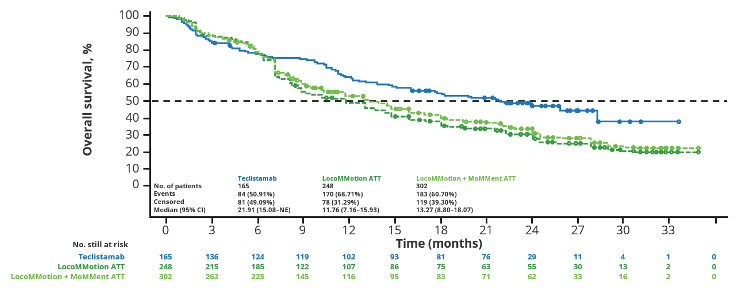
图2 Teclistamab vs LocoMMotion vs LocoMMotion+MoMMent OS率
【结论】与LocoMMotion研究和汇总LocoMMotion + MoMMent研究中真实世界医生选择相比,Teclistamab疗效显著提高,强调了其作为TCE RRMM患者的高效疗法的临床获益。
[P-033] 来自IMF免疫治疗数据库项目的真实世界评估2:Teclistamab可为RRMM患者带来较高的ORR且安全性良好
MajesTEC-1研究结果显示,Teclistamab单药治疗既往接受过重度治疗的RRMM患者缓解率高(63.0%达到≥部分缓解[PR])。IMF免疫治疗小组对Teclistamab在真实世界中RRMM患者的使用进行了跨国学术中心的分析,纳入来自3个国家(美国、希腊、西班牙)6个学术中心接受Teclistamab治疗的患者103例,中位既往治疗线数为6;48.5%(n=50)既往接受过BCMA靶向治疗(CAR-T 33%、抗体偶联药物[ADC] 7%、BsAb 9%);35%的患者(全部在美国)在门诊接受治疗。
41%的患者发生3/4级
中位随访6.4个月时,ORR为67%(图3),6个月PFS率为86%。
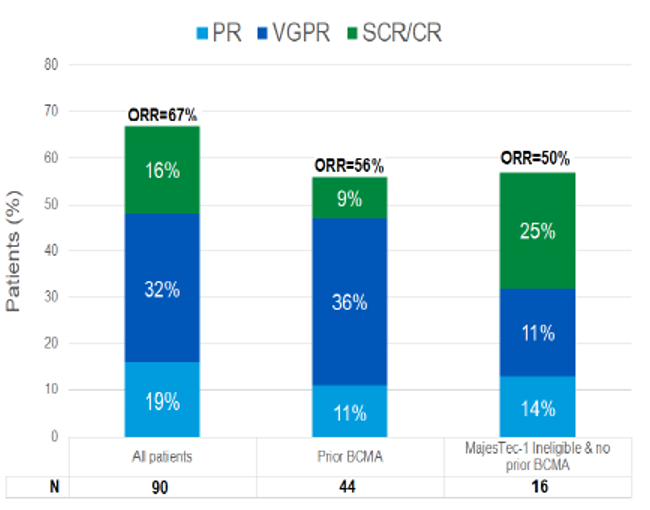
图3 Teclistamab治疗RRMM缓解率
【结论】Teclistamab在真实世界评估中,疗效与MajesTEC-1研究结果相似。CRS发生率与MajesTEC-1研究相似,未发现其他新增安全性事件,感染发生率较低。
[P023] MonumenTAL-1研究患者亚组分析3:Talquetamab治疗RRMM具有良好疗效和安全性
Talquetamab是首个获批的GPRC5D×CD3双特异性抗体。在开放标签、I/II期、单臂MonumenTAL-1研究中,Talquetamab治疗RRMM患者具有良好疗效(ORR>71%)和可控的安全性。研究者分析了Talquetamab在临床相关亚组RRMM患者的疗效和安全性。
对年龄≥75岁、细胞遗传学高危[del(17p)、t(4;14)和/或t(14;16)]、ISS III期、肾功能损害(基线功能≤60mL/min/1.73m2)、三类药物难治(蛋白酶体抑制剂、免疫调节药物和CD38单抗)、髓外病变(EMD)(≥1,包括软组织浆细胞瘤)和既往BCMA暴露的患者亚组进行评估。
截至2023年1月17日,接受RP2D剂量0.4 mg/kg(QW)和0.8 mg/kg(Q2W)Talquetamab治疗的患者分别为143例和145例。
除EMD亚组外,各高危亚组缓解率与总体人群一致(图4,图5)。但在QW和Q2W队列中,EMD亚组缓解率均超过40%。
DOR和PFS在细胞遗传学高危和标危患者中相似,QW和Q2W队列中高危亚组安全性与总体人群一致。

图4 Talquetamab治疗各亚组DOR和PFS
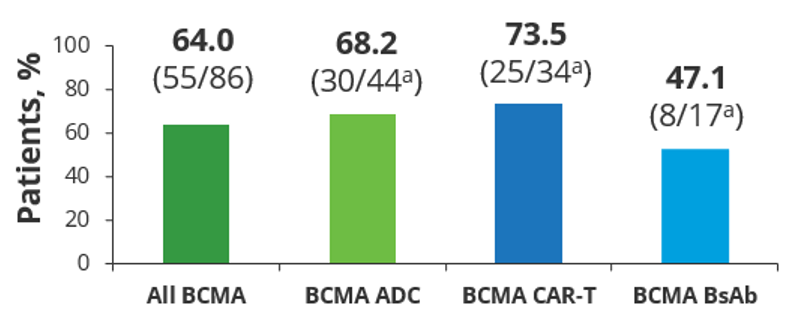
图5 既往BCMA暴露亚组ORR
【结论】Talquetamab单药治疗在大部分细胞遗传学高危的患者以及既往BCMA暴露的患者中显示出高缓解率且安全性可控。
双特异性抗体临床管理
[P-018] 双特异性抗体治疗患者早期感染风险的增加与既往接受BCMA靶向的双特异性抗体或CAR-T治疗无关4
尽管低丙种球蛋白血症和中性粒细胞减少可增加双特异性抗体感染风险,但对于患者早期感染的风险因素仍不确定。
该研究回顾性分析2017年1月至2023年2月期间单中心接受双特异性抗体治疗的所有患者。接受BsAb方案被视为治疗事件(TE),如果患者在12个月内接受两种不同的BsAb方案,则将被视为两种TE。收集每个事件前90天内风险和感染数据的临床预测因素。
队列含90例患者,123个TE(40 BCMA、48 GPRC5D和35 FcRH5方案)。其中有68个TE无感染纪录;其余55个TE在第1-90天内共纪录了77次感染,包括41个感染1次、14个≥2次感染(36次)。
最常见感染是上呼吸道感染(38%),血行感染(15%),肺炎(13%),胃肠道感染(14%),巨细胞病毒(CMV)血症/感染(9%),尿路感染(8%)和皮肤感染(3%)。BCMA靶向治疗前90天内的>1次感染率更高(8.4 vs 17.5%)。
无感染、1次感染和>1次感染队列间的基线特征没有差异,包括高危(HR),EMD,RISS分期,ECOG状态,既往治疗线数。在治疗参数方面,3组中性粒细胞绝对值(ANC)、第一天淋巴细胞绝对值(ALC)、IgG水平、接受IVIG、CRS分级、托珠单抗使用和类固醇治疗剂量也没有差异(0,1和2例感染)。多变量分析显示,接受BCMA与非BCMA BsAb治疗、HRMM、基线时的IgG、既往接受CAR-T治疗或既往接受BCMA靶向治疗等协变量均与感染风险增加无显著相关。
【结论】90天内的早期感染与特定的基线危险因素无关。既往接受免疫治疗不会增加早期感染的风险,IgG水平、ALC和ANC也不是早期感染预测因素。
[NSP-01] 接受新疗法的RRMM感染风险和预防护理途径的更新5
2022年,亨斯迈癌症研究所(HCI)开发了一种护理途径,用于监测接受干细胞移植、CAR-T治疗和BsAB治疗患者的耶氏
定期监测自体移植后、接受CART和BsAb治疗后的MM患者信息:CD4计数、巨细胞病毒拷贝滴度(CMV NAAT)、预防用药、下一次随访。基于报告,护士将(1)开始监测CD4和/或CMV,(2)停止监测CD4和/或CMV,(3)开始PJP预防用药(CD4<200),或(4)停止PJP预防用药(CD4连续两个月>200)。2022年10月,通过NAAT滴度监测BsAb患者的CMV已添加到报告和算法中。如果检测到CMV NAAT但无法量化,则每周进行监测,直到未检测到为止。如果CMV滴度可定量为>100 IU/mL,则开始适当的诱导治疗并每周监测。
治疗持续到未检测到CMV NAAT或直到14天。如果接受CMV治疗的患者无临床症状,一旦无法检测到CMV NAAT,则停止治疗。继续对这些患者进行每月监测。如果CMV转为阳性且患者有症状,则启动感染科会诊以简化干预。
在对高危患者进行一年的密切监测后,HCI没有出现新的PJP感染。在满足每种诊断流程CMV载量监测需求的患者中,12例正在接受双特异性治疗,2例在CAR-T后接受>1剂托珠单抗或地塞米松(≥10mg,持续3天)治疗,并且基线CMV IgG血清阳性。1例无症状患者正在接受BsAB临床试验;其他接受监测患者未达到治疗阈值。
【结论】基于该研究中心更新的算法,其护理实践已经提升到能快速识别PJP和CMV病毒血症的发生,并对风险最高的患者进行适当干预。因此,临床上已减少了因感染而导致治疗时间的延长,从该中心无新发的PJP感染及仅有一小部分轻度CMV患者可以佐证。在未来,希望进一步完善RRMM中CD4和CMV滴度监测及监测的频率。
小结
BsAb是一种新型的骨髓瘤免疫疗法,具有良好的疗效和安全性。随着真实世界临床实践的不断积累,将进一步提高骨髓瘤患者的生存获益及优化临床管理。