
第28届欧洲血液学年会(EHA)将于2023年6月8日-11日在德国法兰克福以线上+线下的形式举行。北京协和医院韩冰教授团队3项关于骨髓增生异常综合征(MDS)、阵发性睡眠性血红蛋白尿症(PNH)以及再生障碍性贫血(AA)的研究入选了2023 EHA会议的壁报,主要内容汇总如下,以飨读者。
摘要号:P716
研究题目:基因表达分析揭示了骨髓间充质干细胞在骨髓增生异常综合征伴环形铁粒幼细胞中的特征
研究背景
骨髓间充质干细胞(BM-MSCs)是骨髓微环境中的关键功能细胞,在MDS中,BM-MSCs增殖缓慢、凋亡数目增加、造血支持能力降低,最终导致造血功能异常。骨髓增生异常综合征伴环形铁粒幼细胞(MDS-RS)是一种具有免疫激活特性的独特MDS亚型,与AA的免疫机制有一些相似之处,但与部分高危MDS亚型,如MDS-EB的免疫机制有显著差异,其遗传学和临床特征可能与骨髓微环境有关。研究者探讨MDS-RS MSCs的基因表达及与其他MDS亚型、AA和健康对照组相比的不同之处,分析表达存在差异的基因对上下游通路的影响并描述其在MDS-RS发病机制中的作用。
研究方法
纳入在北京协和医院确诊的MDS患者、AA患者及健康个体,根据2016年WHO标准进行分类,并提取患者的骨髓血用于BM-MSCs培养,培养至第3代(P3)进行验证。对收集细胞进行转录组测序和差异分析。
研究结果
共纳入11例MDS-RS患者、3例MDS-SLD/MLD患者、4例MDS-EB1/2患者、4例AA患者和5例健康个体。与健康对照组相比,参与蛋白质消化吸收的相关基因在MDS-RS中表达上调,包括COL11A1和其他主要在间质源性肿瘤中表达的基因。这些基因在MDS-SLD/MLD和MDS-EB1/2中也表达上调,但不如MDS-RS上调显著。相较于AA,MDS-RS中LIF、HBEGF等促增殖基因表达上调。与MDS-SLD/MLD相比,MDS-RS中DNA复制相关基因表达较低;而与MDS-EB1/2相比,MDS-RS中DNA复制、DNA修复、细胞增殖、RNA转运等多途径基因表达下调。
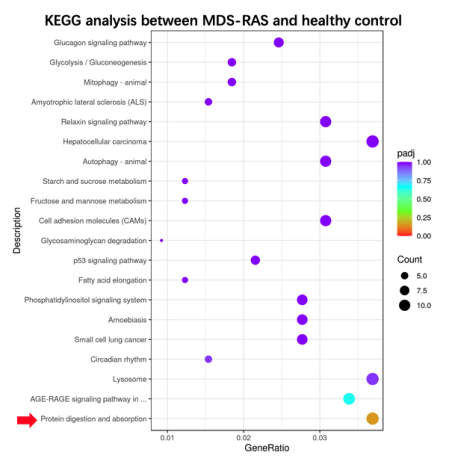
MDS-RAS组与健康对照组的KEGG分析
研究结论
与健康对照组相比,MDS-RS中的BM-MSCs增殖能力增强,来源于间充质谱系的肿瘤相关基因表达上调尤为显著。尽管MDS-RS是一种低危MDS亚型,但此类基因表达上调,虽然这些基因通常存在于间质源性肿瘤,但在MDS-RS中,MSCs充当基质细胞而非恶性细胞,是支持造血功能的微环境的一部分,因此支持作用被增强。将MDS-SLD/MLD和MDS-EB1/2与健康对照组相比,也观察到类似差异,但不如在MDS-RS中差异明显,表明这种现象可能为MDS-RS所特有。
摘要号:P770
研究题目:识别阵发性睡眠性血红蛋白尿症中与增殖和血栓形成相关的基因
研究背景
PIGA基因突变不能完全解释PNH中异常克隆的增殖优势和血栓形成倾向,其他可能发挥作用的基因值得进一步研究。不同研究中血栓形成的高危基因不同,表明基因与临床关系间的复杂性有待进一步研究。研究者尝试分别找到与PNH CD59+和CD59-细胞增殖、免疫调节和血栓形成调节相关的可能基因,并在更大的PNH队列中进行验证。
研究方法
对6例PNH患者的CD59+和CD59-外周血白细胞进行分组,并分别进行全外显子组测序(WES)和全转录组测序(WTS)。选择6名年龄、性别匹配的健康志愿者作为对照。通过基因本体(GO)分析挑选出与增殖、凋亡、免疫和血栓形成相关的基因。随后在40例PNH患者的WES结果中识别出所选基因,最后在另外40例PNH患者中采用Sanger法进行验证,以确定目标基因。对7例患者的CD59+和CD59-白细胞进行分组,并分别通过Q-PCR、流式细胞术和蛋白质印迹法进一步验证这些目标基因的RNA和蛋白表达。最终选择的基因与临床特征相关。
研究结果
CD59+和CD59-细胞中T细胞活化相关基因表达上调,血小板脱颗粒、凝血、止血、白细胞增殖、血小板活化相关基因表达下调,相较于CD59-细胞,CD59+细胞中白细胞增殖、血小板活化、凝血调节相关基因表达进一步下调(P<0.05)。对于最终选择的候选基因,PNH克隆11%-20%的患者NRP1和FLT1基因突变发生率更高(P=0.01)。PNH克隆11%-85%的患者SELP、vWF和EpHB2基因突变发生率更高(P=0.03)。与典型PNH患者相比,BMF/PNH患者SWAP70、SLC15A4或ABCA13基因突变发生率更高(P=0.02)。血栓患者EpHB2基因突变的发生率较高,SELP基因突变的发生率较低(P<0.05)。
研究结论
PNH患者T细胞活化相关基因表达上调,增殖和凝血相关基因表达下调,并且CD59+细胞增殖和血栓形成调节基因表达进一步下调。其他基因可能与PNH增殖和凝血障碍有关。
摘要号:P784
研究题目:环孢素联合血小板生成素受体激动剂联合或不联合抗胸腺细胞球蛋白治疗再生障碍性贫血患者:一项多中心真实世界回顾性研究
研究背景
获得性AA主要是一种免疫介导的骨髓衰竭性疾病。免疫抑制治疗(IST)是不适合造血干细胞移植AA患者的一线治疗方法。抗胸腺细胞球蛋白(ATG)联合环孢素(CsA)的标准IST治疗使重型再生障碍性贫血(SAA)患者的血液学缓解率达60%-80%。艾曲泊帕(EPAG)对复发难治的AA患者显示出一定的疗效,ATG联合CsA和EPAG作为SAA患者的一线治疗方案,有效率高达94%。在标准IST的基础上加入EPAG可提高SAA患者的血液学缓解率、血液学缓解速度和血液学缓解深度。
目前,ATG仍然是SAA患者及输血依赖型非重型再生障碍性贫血(TD-NSAA)患者的首选治疗方案。然而,在中国,由于许多中心缺乏相关经验,入院困难,治疗费用高昂,患者住院时间长,副作用相对严重,ATG应用较少。一项涉及中国22个AA中心的前瞻性注册研究显示,只有22.2%的新诊断AA患者(SAA或TDAA)接受了指南推荐的标准IST(包括ATG)。EPAG对AA患者均具有良好的疗效和安全性,CsA联合EPAG可能是一种合适的替代方案。研究者回顾性收集了来自多中心的曾接受CsA+ATG+EPAG或CsA+EPAG治疗的新诊断AA患者的数据,并计划比较这两种治疗方案在真实世界中的疗效、副作用和结果。
研究方法
研究纳入中国北方地区13个医学中心既往未经治疗的成年AA患者,并将这些患者分为ATG联合CsA+EPAG组(A组)与CsA+EPAG组(B组),比较了所有患者和不同疾病严重程度亚组的疗效和安全性,分析了可能影响有效率的因素。
研究结果
共纳入89例患者,A组51例,B组38例。EPAG的中位起始剂量和最大剂量分别为50mg,qd和75mg,qd。A组和B组中患者6个月总缓解率(ORR)/完全缓解(CR)率分别为73.3%/24.4%和60.6%/27.3%(P>0.1)。A组和B组中SAA患者6个月ORR为74.1%vs.50%,6个月CR率为25.9%vs.20%(P>0.1)。
多变量分析显示,性别显著影响患者6个月ORR(P=0.017,OR 6.045,95% CI:1.377-26.546),从发病到治疗的时间显著影响患者12个月CR率(P=0.026,OR 0.263,95% CI:0.081-0.852)。接受CsA+EPAG治疗的NSAA患者和SAA患者6个月ORR为75.0%vs.52.4%,CR率为41.7%vs.19.0%(P>0.1)。多变量分析显示,只有性别显著影响B组患者6个月ORR(P=0.047,OR 10.754,95% CI:1.031-112.124)。除输注ATG过程中出现的反应及血清病外,两组副作用的发生率无明显差异(P>0.05)。A组患者死亡率为7.8%(4/51),B组没有患者死亡(P>0.1)。
研究结论
在新诊断的AA患者中,CsA联合EPAG与标准IST联合EPAG相比疗效和副作用相似。