
骨髓增生异常综合症(MDS)是一组起源于造血干细胞的肿瘤性疾病,主要特征是骨髓造血功能异常、血细胞发育异常,表现为难治性的血细胞减少、造血功能衰竭,并且高风险向急性白血病转化,曾被称为白血病前期。2019年12月7日至10日在美国奥兰多举行的第61届美国血液学会(ASH)年会上,发布了口服Rigosertib联合阿扎胞苷(AZA)作为高危骨髓增生异常综合征(HR-MDS)患者一线治疗的II期研究结果。
研究背景
阿扎胞苷(AZA)单药治疗已被证实可改善HR-MDS患者的总生存期(OS),仅部分患者可获得临床上有意义且持久的疗效(Silverman 2006)。显而易见的治疗策略是开发一种两药方案,该联合药物在HR-MDS患者中单药有效,且可以与AZA安全有效地联合用药。几种药物已与AZA联合用于HR-MDS患者的一线治疗,总缓解率(ORR)和完全缓解(CR)/部分缓解(PR)率与AZA单药治疗相当(ORR为38%,CR/PR为24%)(Ades ASH 2018; Sekeres JCO 2017)。
Ras途径中的RAS和其他信号分子在HR-MDS患者中经常发生突变,并被认为可以驱动白血病转化(Takahashi 2013)。Rigosertib可以干扰RAF激酶的RAS结合结构域并抑制RAS-RAF-MEK和PI3Ks途径(Athuluri-Divakar,Cell 2016),因此该药是一个与AZA联合的候选药物。此外,rigosertib与AZA在体外联合可协同抑制白血病细胞的生长并诱导其凋亡(Skiddan AACR 2006)。本文报告了一项患者接受口服rigosertib联合标准剂量AZA治疗作为HR-MDS一线治疗的II期研究的最新结果。
研究方法
在II期研究09-08中,共有39例初治HR-MDS/RAEB-t(转化型难治性贫血伴原始细胞增多)患者,接受了口服rigosertib联合标准剂量AZA的治疗。Rigosertib的剂量为840 mg/天(早晨560 mg,下午280mg)或1120mg /天(早晨560 mg,下午560mg或早晨840 mg,下午280 mg)(Maniar ASH 2018)。根据2006 IWG标准确定疗效,包括输血独立性(56天内无外周血细胞及血小板输入)。口服rigosertib于每1周期(28天)的第1-21天给药。从第8天开始,胃肠外给药AZA 75 mg/m2/天,持续7天。如果患者接受了3个周期的治疗,则可以评估疗效。
研究结果
患者的中位年龄为64岁(范围是42-90岁)。 研究入组时9例患者的IPSS-R评分为“中危”,8例是高危,17例是极高危。在研究开始时,共有20例患者有输血依赖。在所有IPSS-R细胞遗传学预后亚组中均观察到CR/PR:极高危组60%,高危组25%,中危组37.5%和低危组25%。在所有有较高IPSS-R预后风险评分的患者中也观察到CR/PR:极高危组42%,高危组17%和中危组25%。临床获益/风险的概况见表1.
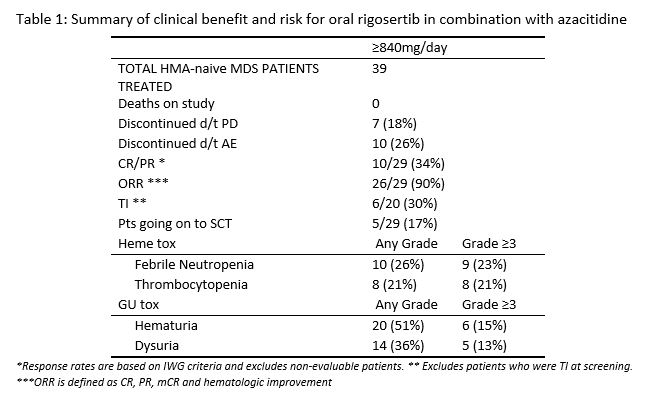
中位缓解持续时间为12.2个月(0.1-24.2 +),中位治疗持续时间为8个月(1.3-27.3)。获得首次和最佳缓解的时间为1/4个月。4例患者治疗仍有疗效。
10例不良事件导致D/C:尿路疼痛(2例),尿潴留、血尿、肾积水、溶骨病变、脑出血、白细胞计数减少、中性粒细胞计数减少和腹部疼痛各1例。表1中最常见的不良事件与既往报道的rigosertib和AZA单药治疗的不良事件相似,并且使用特定的管理指南减轻了GU毒性。大多数经历≥2级不良事件的MDS患者均得到妥善处理,并继续接受两药方案治疗。
结论
作为去甲基化药物(HMA)初治HR-MDS患者的一线治疗,口服rigosertib联合AZA的疗效(ORR为90%,CR率为34%)和安全性良好,并且与标准剂量AZA单药治疗的历史结果相当(ORR为38%,CR率<20%)。HR-MDS 患者中30%的输血独立性(TI)具有临床意义,但需要在大型随机III期研究中予以证实。
口服rigosertib联合AZA的耐受性良好,现已重复使用两年以上。由于rigosertib是口服制剂,与AZA有协同作用,无叠加毒性,因此rigosertib是AZA联合用药的理想选择。基于疗效结果和良好的安全性,计划在HMA初治HR-MDS患者中进行关键的III期试验。